Водневий показник розчинів солей – Протолітична рівновага
КИСЛОТИ Й ОСНОВИ
2. Протолітична рівновага
2.4. Водневий показник розчинів солей
Багато сольових розчинів мають нейтральне середовище, деякі – кисле або лужне. За Бренстедом, вода при цьому виконує функцію основи або кислоти.
Приклад. Натрій хлорид
Іон Na+: не вступає в реакцію з водою.
Іон Сl-: надзвичайно слабка основа, тому протоліз не відбувається.
Розчин натрій хлориду має нейтральне середовище.
Приклад. Амоній хлорид Іон NH4+: реагує з водою як слабка кислота
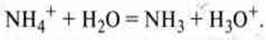
Іон СІ-: дуже слабка основа, тому протоліз не відбувається.
Розчин амоній хлориду має кисле середовище.
Приклад. Натрій карбонат
Іон Na+: не вступає в реакцію з водою./o:p>
Іон СО32-: реагує з водою як слабка основа:
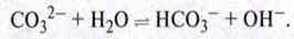
Розчин натрій карбонату має лужне середовище.
Реакцію солей з водою називають гідролізом. До того ж залежно від хімічної природи іонів солі утворюються кислі або лужні розчини.
Related posts:
- Водневий показник – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.2. Водневий показник У водних розчинах електролітів (кислот, основ) іонний добуток води залишається практично незмінним, поки їх концентрація не стане дуже великою. Отже, якщо концентрація с(Н3О+) у розчині більша, ніж у чистій воді, то с(ОН-) повинна бути менша, і навпаки. Приклад. Рівновага НСl + Н2O Н3O+ + Сl – […]...
- Водневий показник розчинів слабких кислот і основ – Сила кислот і основ – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.3. Сила кислот і основ Водневий показник розчинів слабких кислот і основ Оскільки при протолізі кислоти чи основи утворюється рівна кількість позитивних і негативних іонів, їхня концентрація буде однаковою: Якщо в даних рівняннях прологарифмувати значення концентрацій іонів (Н3О+) і (ОН-), то одержимо значення pH розчину кислоти або значення рОН […]...
- Значення pH буферів – Буферні розчини – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.5. Буферні розчини Суміш слабкої кислоти і зв’язаної основи, або слабкої основи і її зв’язаної кислоти характеризується тим, що її водневий показник при додаванні не дуже великої кількості іонів гідроксонію або гідроксид-іонів практично не змінюється. Розчини, показник pH яких по відношенню до кислот і лугів залишається стабільним, називають буферними […]...
- Слабкі кислоти й основи – Сила кислот і основ – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.3. Сила кислот і основ Слабкі кислоти й основи У слабких кислот і основ дисоціація є неповною. Внаслідок цього в розчині є недисоційовані молекули. Тому показник pH неможливо розрахувати лише з концентрації кислоти або основи. Додатково потрібна інформація про стан протолітичної рівноваги: Оскільки в цьому випадку концентрація молекул води […]...
- Сильні кислоти й основи – Сила кислот і основ – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.3. Сила кислот і основ Силу кислоти або основи, за Бренстедом, визначають здатністю до протолізу, що залежить від того, як сильно виражена готовність речовини віддавати або приймати протони. Реагент визначає, яку функцію – кислоти чи основи – виконує речовина в реакції. У цьому випадку важливим реагентом є вода, оскільки […]...
- Дія буферів – Буферні розчини – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага 2.5. Буферні розчини Дія буферів Використовуючи константу рівноваги процесу дисоціації кислоти, можна показати дію буфера: – Додавання кислоти, тобто збільшення с(Н3О+). Для збереження рівноваги додані іони гідроксонію реагуватимуть з відповідними іонами А-, утворюючи недисоційовану НА, практично не змінюючи концентрацію іонів гідроксонію. – Додавання лугу, тобто збільшення с(ОН-). Додані гідроксид-іони […]...
- Гідроліз солей як окремий випадок реакцій йонного обміну у водних розчинах електролітів ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.11. Гідроліз солей як окремий випадок реакцій йонного обміну у водних розчинах електролітів У хімії часто стикаються з явищем гідролізу1 – хімічної взаємодії речовин з водою. Найбільше практичне значення має гідроліз солей. Гідроліз солей – це хімічна взаємодія солей […]...
- Нейтралізація слабких кислот і основ – Нейтралізація КИСЛОТИ Й ОСНОВИ 3. Нейтралізація При змішуванні рівних об’ємів соляної кислоти і розчину їдкого натру однакових концентрацій, утворюється нейтральний розчин натрій хлориду, що має показник pH = 7. Таким чином, кислотні і лужні властивості початкових речовин нейтралізуються. Нейтралізація є реакцією взаємодії іонів гідроксонію і гідроксид-іонів з утворенням молекул води: Н3О+ + ОН – 2 Н2О. […]...
- Теорія Бренстеда – Визначення кислот і основ КИСЛОТИ Й ОСНОВИ 1. Визначення кислот і основ 1.2. Теорія Бренстеда Багато речовин утворюють кислі або лужні розчини, але не відповідають наведеним визначенням кислот і лугів. Приклад. Розчин амоній хлориду має кислу реакцію, а розчин натрій ацетату – лужну. У зв’язку з цим Йоганн Бренстед і Томас Лоурі сформулювали в 1923 р. нове визначення кислот […]...
- Загальні способи добування металів. Електроліз розплавів солей і лугів – Метали Хімія Неорганічна хімія Метали Загальні способи добування металів. Електроліз розплавів солей і лугів Металургія – це галузь промисловості, яка займається видобуванням металів із руд. Електроліз – окисно-відновний процес, що відбувається на електродах під час проходження електричного струму через розплав або розчин електроліту. Якщо в розплав електроліту, наприклад натрій хлориду, занурити інертні електроди й пропускати постійний […]...
- Іонний добуток води – Протолітична рівновага КИСЛОТИ Й ОСНОВИ 2. Протолітична рівновага Рівновага, яка виникає в процесі протолізу, залежить від температури, хімічної природи реагентів і зміщується в бік утворення стійкіших сполук. 2.1. Іонний добуток води Молекула води, згідно теорії Бренстеда, може виступати як кислота або як основа. І навіть у чистій воді відбувається так званий автопротоліз (грец. autos – сам): Проте […]...
- ГІДРОЛІЗ СОЛЕЙ – ВУГЛЕЦЬ І ЙОГО СПОЛУКИ Хімія – універсальний довідник ВУГЛЕЦЬ І ЙОГО СПОЛУКИ ГІДРОЛІЗ СОЛЕЙ У нейтральних розчинах, тобто за відсутності кислот і лугів, у результаті дисоціації (дуже слабкої) води утворюються однакові кількості іонів Н+ і ОН-: Додавання до води кислоти збільшує концентрацію іонів Н+ і, зміщуючи рівновагу дисоціації води вліво, знижує концентрацію іонів ОН-. Отже, кислий розчин містить більше […]...
- Дисоціація води. Водневий показник ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.8. Дисоціація води. Водневий показник Хімічно чиста вода дуже слабо проводить електричний струм. Провідність зумовлена дисоціацією: За температури 25 °С ступінь дисоціації води а = 1,8 · 10-9. Оскільки 1 л води (1000 г) містить 55,56 моль речовини, концентрації […]...
- Електроліз водних розчинів електролітів (кислот, основ, солей) – Електроліз ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 6. Суміші речовин. Розчини 6.13. Електроліз 6.13.2. Електроліз водних розчинів електролітів (кислот, основ, солей) Під час електролізу водних розчинів електролітів, крім катіонів і аніонів розчиненої речовини, у процесах окиснення і відновлення, що відбуваються на електродах, можуть брати участь молекули води. При цьому можуть […]...
- Зворотність реакції – Рушійна сила хімічних реакцій ЕНЕРГЕТИКА ХІМІЧНИХ РЕАКЦІЙ 3. Рушійна сила хімічних реакцій 3.5 . Зворотність реакції Відповідно до рівняння Гіббса-Гельмгольца, вільна енергія реакції ∆G0R залежить від температури. Якщо не враховувати залежність температури від ∆H0R і ∆S0R, то рівняння Гіббса-Гельмгольца відповідає рівнянню прямої. Залежно від знаків ∆H0R і ∆S0R розрізняють чотири типи реакції. Тип 1: при температурі Т < Т0 […]...
- Добуток розчинності – Рівновага розчинності ХІМІЧНА РІВНОВАГА 3. Рівновага розчинності 3.2 . Добуток розчинності Якщо до насиченого розчину солі у воді ще додати цю ж сіль, то ця добавка випаде в нерозчинений осад. Якщо до нього додати сіль, що містить один з іонів розчиненої солі, то утвориться такий самий осад. Приклад. Якщо до насиченого розчину кальцій сульфату додати трохи кальцій […]...
- Протолітична теорія кислот і основ – РОЗЧИНИ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 5. РОЗЧИНИ. ТЕОРІЯ ЕЛЕКТРОЛІТИЧНОЇ ДИСОЦІАЦІЇ § 5.13. Протолітична теорія кислот і основ Теорія електролітичної дисоціації пояснила численні явища і процеси, що відбуваються у водних розчинах електролітів. Так, наприклад, у різних реакціях нейтралізації NaOH + НСl = NaCl + Н2O; КОН + […]...
- Йонний зв’язок – Йонний, металічний і водневий зв’язки ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 3. Хімічний зв’язок 3.7. Йонний, металічний і водневий зв’язки 3.7.1. Йонний зв’язок Якщо різниця електронегативностей пари атомів, що утворюють зв’язок, > 1,7 (за Полінгом), між ними утворюється йонний зв’язок. Зазвичай йонний зв’язок утворюється між металічними і неметалічними елементами. Атоми металічних елементів віддають електрони […]...
- Гідроліз солей – НАЙВАЖЛИВІШІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 6. НАЙВАЖЛИВІШІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК § 6.5. Гідроліз солей Означення. Досвід показує, що розчини середніх солей мають лужну, кислу або нейтральну реакцію, хоча вони і не містять ні водневих, ні гідроксильних іонів. Пояснення цьому факту слід шукати у взаємодії солей з […]...
- Електроліз розчинів та розплавів електролітів – ОКИСНО-ВІДНОВНІ ПРОЦЕСИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ ОКИСНО-ВІДНОВНІ ПРОЦЕСИ Електроліз розчинів та розплавів електролітів Сукупність ОВР, які протікають на електродах у розчинах та розплавах електролітів при пропусканні через них електричного струму, називають електролізом. На підставі етимології слова можна сказати, що електроліз (від електро… і грец. лізіс – розклад) – це […]...
- Водневий зв’язок – Йонний, металічний і водневий зв’язки ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ 3. Хімічний зв’язок 3.7. Йонний, металічний і водневий зв’язки 3.7.3. Водневий зв’язок Низка сполук з полярним Ковалейтним зв’язком, які містять Гідроген і елемент з високою електронегативністю (найчастіше Оксиген, Флуор, Нітроген), утворюють так званий водневий зв’язок (позначають “—“). Це різновид невалентного міжмолекулярного зв’язку (вандерваальсового1), […]...
- Гідроліз солей РОЗДІЛ 1 ПОВТОРЕННЯ ТА ПОГЛИБЛЕННЯ ТЕОРЕТИЧНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ § 13. Гідроліз солей Усвідомлення змісту цього параграфа дає змогу: Пояснювати поняття “гідроліз солей” і суть цього процесу; характеризувати різні випадки гідролізу; Вміти наводити приклади гідролізу і складати рівняння відповідних реакцій; Прогнозувати реакцію середовища та експериментально її визначати. Пригадайте, які речовини називаються солями та […]...
- Електроліз водних розчинів електролітів – ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ Частина І. ЗАГАЛЬНА ХІМІЯ Розділ 7. ОКИСНО-ВІДНОВНІ РЕАКЦІЇ. ЕЛЕКТРОЛІЗ § 7.7. Електроліз водних розчинів електролітів Слід розрізняти електроліз розплавлених електролітів і їх розчинів. В останньому випадку в процесах можуть брати участь молекули води. Як приклад розглянемо електроліз концентрованого водного розчину хлориду натрію (електроди вугільні). В цьому […]...
- ГІДРОЛІЗ СОЛЕЙ Хімія – універсальний довідник ХІМІЧНИЙ ПРОЦЕС ХІМІЧНА РІВНОВАГА ГІДРОЛІЗ СОЛЕЙ Гідроліз солі – обмінна реакція між сіллю і водою. Схема гідролізу за катіоном: Гідролізу за катіоном підлягають солі слабкої основи і сильної кислоти: Чим більший заряд і менші розміри катіона, тим більший ступінь гідролізу. Схема гідролізу за аніоном: Чим більший негативний заряд і менший розмір […]...
- Електролітична дисоціація кислот, основ, солей у водних розчинах Тема 1 РОЗЧИНИ Урок 12 Тема уроку. Електролітична дисоціація кислот, основ, солей у водних розчинах Цілі уроку: поглибити знання учнів про електролітичну дисоціацію на прикладі розчинів кислот, основ і солей; формувати навички складання рівнянь дисоціації на прикладі розчинних кислот, основ, солей; уточнити визначення кислот, основ і солей у світлі теорії електролітичної дисоціації. Тип уроку: засвоєння […]...
- Загальні способи одержання оксидів, основ, кислот, солей Тема 2 ОСНОВНІ КЛАСИ НЕОРГАНІЧНИХ СПОЛУК УРОК 34 Тема. Загальні способи одержання оксидів, основ, кислот, солей Цілі уроку: розвивати вміння й навички учнів у складанні рівнянь на прикладі одержання оксидів, основ, кислот, солей; систематизувати знання учнів про загальні способи одержання оксидів, основ, кислот і солей; показати їх взаємозв’язок з генетичним зв’язком класів неорганічних сполук. Тип […]...
- Приготування розчинів Тема 1 РОЗЧИНИ Урок 9 Тема уроку. Приготування розчинів Цілі уроку: формування навичок і вмінь приготування розчинів; розвиток навичок розв’язання задач із використанням поняття “масова частка розчиненої речовини”, розрахунків, пов’язаних із приготуванням розчинів. Тип уроку: застосування вмінь і навичок. Форми роботи: самостійна робота під керівництвом учителя, виконання тренувальних завдань. Обладнання: таблиця розчинності, картки-завдання. ХІД УРОКУ […]...
- Кількісний склад розчину. Масова частка розчиненої речовини. Приготування розчинів Тема 1 РОЗЧИНИ Урок 7 Тема уроку. Кількісний склад розчину. Масова частка розчиненої речовини. Приготування розчинів Цілі уроку: ознайомити учнів зі способами вираження складу розчинів, поняттями “масова частка розчиненої речовини”, “концентрація”; формувати навички використання цих понять для обчислень і приготування розчинів. Тип уроку: формування нових знань, умінь і навичок. Форми роботи: фронтальна бесіда, розв’язання задач. […]...
- Способи кількісного вираження складу розчинів – РОЗЧИНИ Хімія підготовка до ЗНО та ДПА Комплексне видання ЧАСТИНА І ЗАГАЛЬНА ХІМІЯ РОЗЧИНИ Способи кількісного вираження складу розчинів Для кількісного опису складу розчину часто вживають величини: масова частка розчиненої речовини й молярність розчину. Окрім цих, є й менш популярні способи: мольна частка, моляльність, нормальність, титр, об’ємна частка тощо. Способів вираження концентрації досить багато, тому що […]...
- Кількісний склад розчинів РОЗДІЛ 1 ПОВТОРЕННЯ ТА ПОГЛИБЛЕННЯ ТЕОРЕТИЧНИХ ПИТАНЬ КУРСУ ХІМІЇ ОСНОВНОЇ ШКОЛИ § 12. Кількісний склад розчинів Усвідомлення змісту цього параграфа дає змогу: Пояснювати поняття “молярна концентрація”, “масова частка” розчиненої речовини; Вміти визначати зазначені поняття, обчислювати склад розчинів і виготовляти розчини з певною молярною концентрацією розчиненої речовини. Кількісний склад розчинів найчастіше виражається безрозмірною відносною величиною – […]...