Жири. Склад жирів, їх утворення. Жири в природі. Біологічна роль жирів
Тема 3
НАЙВАЖЛИВІШІ ОРГАНІЧНІ СПОЛУКИ
Урок 50
Тема уроку. Жири. Склад жирів, їх утворення. Жири в природі. Біологічна роль жирів
Цілі уроку: формувати знання учнів про склад жирів, їх утворення; з’ясувати їх будову і властивості як естерів гліцерину та вищих карбонових кислот; ознайомити учнів з хімічними властивостями жирів на прикладі гідролізу й гідрування; показати поширення жирів у природі, їх біологічну роль, застосування.
Тип уроку: комбінований урок засвоєння знань, умінь і навичок і творчого застосування їх на практиці.
Форми
Обладнання: зразки жирів рослинного і тваринного походження.
ХІД УРОКУ
I. Організація класу
II. Перевірка домашнього завдання.
Актуалізація опорних знань
1. Перевірка домашнього завдання
2. Повідомлення учнів про біологічну роль жирів
III. Вивчення нового матеріалу
Жири як естери гліцерину й вищих карбонових кислот
1. Розповідь учителя
Жири – естери гліцерину й вищих карбонових кислот.
Крім основного складу, жир містить близько 4 % нежирних речовин, пігменти, вітаміни А, D, Е, К і низькомолекулярні кислоти.
Загальна формула
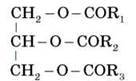
Де R1, R2, R3 – радикали кислот, що містять від 3 до 2B атомів Карбону.
2. Класифікація жирів
(Заповнюємо з учнями схему; учні самостійно наводять приклади, роблять висновки щодо застосування жирів, роблять повідомлення про поширення жирів у природі.)
За походженням:
– рослинні (олії);
– тваринні;
– комбіновані.
Наведіть приклади жирів рослинного й тваринного походження. За консистенцією:
– тверді (утворені насиченими вищими карбоновими кислотами);
– рідкі (утворені ненасиченими вищими карбоновими кислотами). Наведіть приклади насичених і ненасичених вищих карбонових кислот.
До складу природних жирів входять вищі карбонові кислоти з парним числом атомів Карбону:
– пальмітинова C15H31COOH;
– стеаринова C17H35COOH;
– олеїнова C17H33COOH;
– лінолева C17H31COH;
– ліноленова C17H29COOH.
Наприклад:
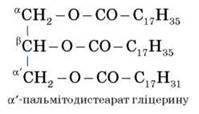
Загальна назва жирів – тригліцериди.
Приклади природних жирів
– Вершкове масло: олео-пальміно-бутират
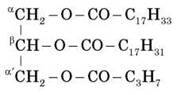
– Свиняче сало: олео-пальміно-стеарат
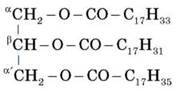
– Лляна олія: 61,6 % гліцеридів лінолевої кислоти.
– Соняшникова, горіхова олії: 30-B0 % гліцеридів лінолевої кислоти, решта – олеїнової кислоти.
3. Хімічні властивості
Гідроліз (омилення)
Розповідь учителя
Протікає в присутності каталізаторів (кислот, лугів, оксидів Магнію, Кальцію, Цинку).
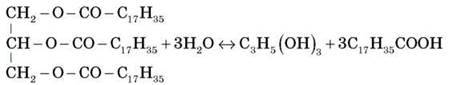
Якщо замість води взяти луг, то в результаті гідролізу одержують солі вищих карбонових кислот – мила (тверде – натрієве, рідке – калієве).
Самостійно складіть рівняння омилення жиру:
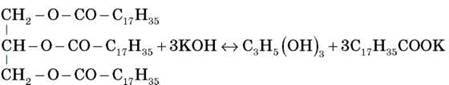
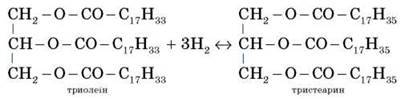
Промислове значення має реакція гідрування жирів. У результаті рідкі жири (такі, що містять ненасичені кислоти) перетворюються на тверді (які містять лише насичені кислоти).
4. Повідомлення учнів про застосування жирів
IV. Первинне застосування отриманих знань (керована практика)
Завдання 1. Обчисліть маси натрій гідроксиду й жиру (тригліцериду стеаринової кислоти), які необхідно взяти для одержання 100 кг натрієвого мила. Втрати у виробництві становлять 20 %.
Завдання 2. Обчисліть об’єм водню (у перерахуванні на н. у.), який необхідно витратити на перетворення 1 т рослинної олії (умовно прийняти триолеїну) на твердий жир.
Завдання 3. Якщо на розчин мила подіяти сульфатною кислотою, то на поверхні спливає тверда нерозчинна у воді речовина. Складіть рівняння реакції, що протікає.
Завдання 4. У пробірку з речовинами: а) водою; б) водним розчином мила; в) бензином; г) лугом, додали жир і ретельно перемішали. У яких випадках жир розчинився? Чому?
V. Підбиття підсумків уроку
Підбиваємо підсумки уроку, оцінюємо роботу учнів на уроці.
VI. Домашнє завдання
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
Творче завдання. Подумайте й запропонуйте заходи щодо охорони навколишнього середовища від забруднення мийними засобами.