Білки
Тема 3
НАЙВАЖЛИВІШІ ОРГАНІЧНІ СПОЛУКИ
Урок 57
Тема уроку. Білки
Цілі уроку: формувати поняття про білки як природні полімери, первинну, вторинну, третинну й четвертинну структури білкових молекул; ознайомити учнів з фізичними й хімічними властивостями білків на прикладі гідролізу й денатурації; показати кольорові реакції білків як якісні реакції на білки; формувати уявлення про матеріальну єдність світу; дати діалектичні уявлення про організацію речовини від простої до складної на прикладі білків.
Тип уроку: комбінований
Форми роботи: евристична бесіда, розповідь учителя, демонстраційний експеримент.
Обладнання: мультимедійна схема структури білкової молекули.
Демонстрація 17. Денатурація білків.
Демонстрація 18. Кольорові реакції білків.
Лабораторний дослід 14. “Розчинення й осадження білків.
ХІД УРОКУ
I. Організація класу
II. Актуалізація опорних знань. Мотивація навчальної діяльності
Фронтальна бесіда
1) Які функціональні групи входять до складу амінокислот?
2) Складіть схему одержання амінооцтової кислоти
3) Складіть схему утворення дипептиду з аланіну й цистеїну. Який зв’язок називається пептидним?
4) Скільки трипептидів можна одержати шляхом сполучення трьох різних амінокислотних залишків?
Самостійно виберіть із таблиці три амінокислоти та складіть формули утворених ними трипептидів.
III. Вивчення нового матеріалу
Білки – природні полімери 1. Будова білкової макромолекули
Розповідь учителя
Білки (поліпептиди) – природні високомолекулярні нітрогеновмісні органічні сполуки (біополімери), побудовані із залишків а-амінокислот, з’єднаних пептидними (амідними) зв’язками.
Формальне утворення білкової макромолекули можна представити як реакцію поліконденсації?-амінокислот:
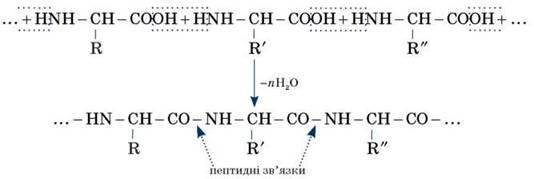
Під час взаємодії двох молекул а-амінокислот відбувається реакція між аміногрупою однієї молекули й карбоксильною групою іншої. це приводить до утворення дипептиду, наприклад:
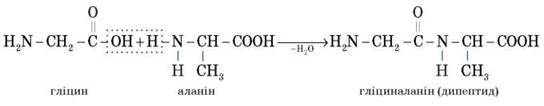
Слід зазначити, що за штучних умов (поза організмом) дві різні амінокислоти можуть утворити чотири ізомерні дипептиди (у цьому випадку – гліциналанін, аланілгліцин, аланілаланін і гліцил-гліцин).
Із трьох молекул а-амінокислот (гліцин + аланін + гліцин) можна одержати трипептид:
H2N – CH2CO – NH – CH(CH3) – CO – NH – CH2COOH
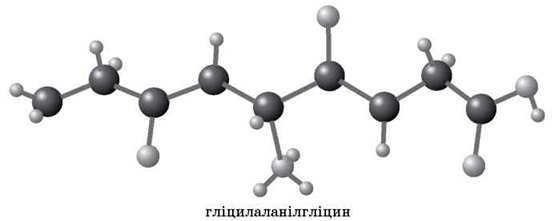
Аналогічно відбувається утворення тетра-, пента – і поліпептидів.
Молекулярні маси різних білків (поліпептидів) становлять від 10 тисяч до кількох мільйонів. макромолекули білків мають стереорегулярну будову, винятково важливу для прояву ними певних біологічних властивостей. Незважаючи на численність білків, до їх складу входять залишки не більш ніж 22 ?-амінокислот.
Різноманітні функції білків визначаються?-амінокислотним складом і будовою їх високоорганізованих макромолекул.
Виокремлюють чотири рівні структурної організації білків (див. рис. на наступній сторінці).
2. Хімічні властивості білків
1) Гідроліз білків
Полягає в гідролізі поліпептидного ланцюга з утворенням набору амінокислот, які утворюють цей поліпептидний ланцюг.
2) Демонстрація 17. Денатурація білків
Денатурація – руйнування третинної та вторинної структур білкової молекули під дією нагрівання, сильних кислот, лугів, солей важких металів, спиртів, радіації.
На прикладі яєчного білка демонструємо денатурацію в процесі нагрівання, під дією сульфатної кислоти, натрій гідроксиду, спирту.
Первинна структура – певна послідовність?-амінокислотних залишків у поліпептидному ланцюгу
Вторинна структура (?-спіраль)
Вторинна структура – це конформація поліпептидного ланцюга, закріплена численними водневими зв’язками між групами N – H і C = O.
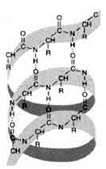
Одна з моделей вторинної структури – ?-спіраль
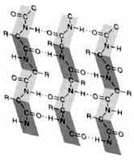
Друга модель – ?-форма (“складчастий лист”), у якій переважають міжланцюгові (міжмолекулярні) водневі зв’язки
Третинна структура
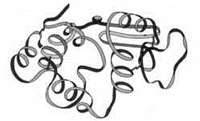
Третинна структура – форма закрученої спіралі в просторі, утвореної в основному за рахунок дисульфідних містків – S – S-, водневих зв’язків, гідрофобних та іонних взаємодій
Четвертинна структура
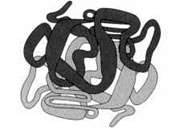
Четвертинна структура – агрегати кількох білкових макромолекул (білкові комплекси), утворені за рахунок взаємодії різних поліпептидних зв’язків
3) Демонстрація 18. Кольорові реакції білків Для білків характерні кольорові реакції, з допомогою яких проводять якісний хімічний аналіз білків.
– Біуретова реакція – дія на білок розчину лугу й розчину купрум(ІІ) сульфату. Розчин набуває фіолетового забарвлення, що вказує на наявність поліпептидних зв’язків.
– Ксантопротеїнова реакція (для білків, що містять бензольне кільце) – дія концентрованої нітратної кислоти з появою жовтого забарвлення. Унаслідок додавання лугу жовте забарвлення змінюється на оранжеве.
– Цистеїнова реакція (для білків, що містять Сульфур) – кип’ятіння розчину білка із плюмбум(ІІ) ацетатом до появи чорного забарвлення.
IV. Первинне застосування одержаних знань (керована практика)
Лабораторна робота 14. Розчинення й осадження білків
1) Яєчний білок поміщаємо в хімічну склянку, додаємо води у співвідношенні 1:1, розмішуємо. Що спостерігаємо? Зробіть висновок про розчинність білка.
2) Наливаємо 1-2 мл одержаного розчину в пробірку. Дотримуючись правил техніки безпеки, нагріваємо до згортання білка.
3) Наливаємо 1-2 мл розчину білка в пробірку, доливаємо 1-2 мл спирту (98 %). Що спостерігаємо?
Зробіть висновок про умови денатурації білка.
V. Підбиття підсумків уроку
Функції білків у природі універсальні:
– каталітичні (ферменти);
– регуляторні (гормони);
– структурні (кератин шерсті, фіброїн шовку, колаген);
– рухові (актин, міозин);
– транспортні (гемоглобін);
– запасні (казеїн, яєчний альбумін);
– захисні (імуноглобуліни) тощо.
Підбиваємо підсумки уроку, оцінюємо роботу учнів на уроці.
VI. Домашнє завдання
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
Творче завдання. Підготувати повідомлення про біологічну роль білків. Чому білкову їжу не можна на тривалий час замінити їжею, що містить лише жири й вуглеводи?