ПЕРІОДИЧНА СИСТЕМА XIМІЧHИХ ЕЛЕМЕНТІВ Д. І. МЕНДЕЛЄЄВА. СТРУКТУРА ПЕРІОДИЧНОЇ СИСТЕМИ
Тема 1 ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ
& 12. ПЕРІОДИЧНА СИСТЕМА XIМІЧHИХ ЕЛЕМЕНТІВ Д. І. МЕНДЕЛЄЄВА. СТРУКТУРА ПЕРІОДИЧНОЇ СИСТЕМИ
Вивчення параграфа допоможе вам:
· ознайомитися зі структурою періодичної системи;
· використовувати періодичну систему хімічних елементів як довідкову для визначення відносної атомної маси хімічних елементів.
Ідея створення періодичної системи належить видатному російському хіміку Дмитру Івановичу Менделєєву й датована 1 березня 1869 року. Вона оформлена у вигляді таблиці, клітинки якої
СТРУКТУРА ПЕРІОДИЧНОЇ СИСТЕМИ. У періодичній системі хімічні елементи розміщені в пронумерованих клітинках. Помер клітинки кожного хімічного елемента невипадковий – він дорівнює заряду ядра атома. Так, заряд ядра атома Оксигену +8 і його порядковий номер теж 8. Періодична система служитиме вам зручною довідкою про хімічні елементи, допомагатиме отримувати
Кожний елемент у періодичній системі має свій порядковий номер. Він є цілим числом і в кожного наступного елемента збільшується на одиницю.
Орієнтуючись на порядкові номери, вкажіть, скільки хімічних елементів міститься в періодичній системі хімічних елементів.
Слід зазначити, що 89 з них трапляються в природі, решту добуто вченими штучно.
Існує декілька варіантів періодичної системи. Та, що зображена на форзаці підручника, складається із семи горизонтальних рядів, що дістали назву періоди. У них чітко простежується збільшення зарядів ядер атомів кожного наступного хімічного елемент а на одиницю.
Переконайтеся в цьому на прикладі 2-го періоду.
Вертикальні стовпчики хімічних елементів періодичної системи дістали назву груп. У зображеній на першому форзаці підручника періодичній системі їх вісім.
ІНФОРМАЦІЯ, ЯКУ НАДАЄ ПОРЯДКОВИЙ НОМЕР ХІМІЧНОГО ЕЛЕМЕНТА. Клітинка періодичної системи, в якій записаний символ хімічного елемента, є місцем постійного його розміщення. Ви вже знаєте, що заряд ядра атома Гідрогену +1. Погляньте на таблицю й ви побачите, що Гідроген розташований у ній під номером 1. З попереднього параграфа вам відомо, що заряд ядра атома Карбону +6. І в періодичній системі цей елемент розміщений у клітинці під номером 6!
Позитивний заряд ядра атома зумовлюють протони. Тож їх кількість дорівнює порядковому номеру хімічного елемента в періодичній системі.
Оскільки протонів й електронів в атомі порівно, то порядковий номер хімічного елемента вказує й на кількість електронів в атомі.
За порядковим номером хімічного елемента можна безпомилково дізнатись, скільки протонів й електронів в атомі.
ІНФОРМАЦІЯ ПРО ВІДНОСНУ АТОМНУ МАСУ ЕЛЕМЕНТА В ПЕРІОДИЧНІЙ СИСТЕМІ. У клітинках з символами хімічних елементів крім порядкових номерів є ще одне число. НИМ позначено відносну атомну масу хімічного елемента. Зверніть увагу, що в більшості елементів вона має дробове значення. Річ у тім, що багато хімічних елементів існують у вигляді кількох стійких різновидів. Відмінність між різновидами атомів одного хімічного елемента полягає в різній кількості нейтронів, тоді як кількість протонів у всіх атомів одного хімічного елемента однакова. Так. Гідроген має 2 стійкі різновиди атомів. Кожний містить по 1 протону в ядрі, а от кількість нейтронів у них різна: в одного їх взагалі немає, у другого є 1 нейтрон. Оскільки маса атома зумовлена масою протонів і нейтронів, то виходить, що відносна атомна маса першого різновиду дорівнює 1, другого – 2. У періодичній системі записана середня відносна атомна маса Гідрогену – 1,00797. Її значення наближене до того різновиду елемента, відсоток атомів якого в природі більший.
Ми будемо з вами користуватися заокругленими до цілого числа відносними атомними масами хімічних елементів за винятком Хлору, що має порядковий номер 17. Для нього загальноприйнятою є відносна атомна маса 35,5.
Узагальнену інформацію про те, яку інформацію внесено до клітинок періодичної системи хімічних елементів, надає мал. 62.
Знайдіть у періодичній системі хімічних елементів клітинка з елементами Карбон, Флуор, Цинк. Для кожного з елементів порівняйте величину порядкового номера а відносної атомної маси. Зробіть висновок про те, що є більшим-порядковий номер чи відносна атомна маса хімічного елемента.
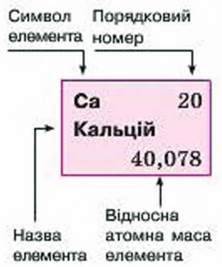
Мал. 52. Інформація про Кальцій з клітинки періодичної системи
За відносною атомною масою та порядковим номером хімічного елемента легко визначити, скільки нейтронів входить до складу ядра атома. Наприклад, ставимо завдання: з’ясувати, скільки протонів і нейтронів містить ядро атома хімічного елемента з порядковим номером 82 та скільки електронів в його атомі.
Знаходимо в періодичній системі клітинку під номером 82. У ній розташований хімічний елемент Плюмбум Рb. Його відносна атомна маса дорівнює 207. Порядковий номер указує на те, що атом має 82 протони й 82 електрони. Заряд ядра атома +82. Здійснивши дію віднімання між числовим значенням відносної атомної маси й порядкового номера хімічного елемента, дізнаємось, скільки нейтронів міститься в ядрі атома Плюмбуму з відносною атомною масою 207:
207 – 82 = 125.
Завдяки тому, що порядковий номер хімічного елемента вказує на важливі його характеристики, періодичною системою хімічних елементів можна користуватися як довідковою для визначення кількості протонів, нейтронів, електронів в атомі, його відносної атомної маси, заряду ядра атома.
Скарбничка ерудита
У періодичній системі хімічні елементи Лантан La з порядковим номером 57 і Актиній Ас з порядковим номером 89 позначені La* й Ас* (див. форзац). Зверніть увагу, що в наступній комірці після Лантану розташований Гафній, порядковий номер якого 72, а не 58. Після Актинію міститься хімічний елемент Резерфордій з порядковим номером 104, а не 90. В обох випадках різниця порядкових номерів наступного й попереднього хімічних елементів дорівнює 14. Саме ця кількість хімічних елементів винесена окремо й названа лантаноїдами та актиноїдами. Це пов’язано з особливостями будови їх атомів, про які ви дізнаєтесь в старших класах.
?
1. Яку інформацію про хімічний елемент містить клітинка періодичної системи, в якій він розташований?
2. Як за допомогою періодичної системи хімічних елементів Д. І. Менделєєва визначити:
А) кількість протонів в ядрі атома;
Б) кількість нейтронів в ядрі атома;
В) скільки електронів має атом?
3. На скільки періодів та груп розподілені хімічні елементи в періодичній системі, зображеній на першому форзаці?
4. Запишіть, інформацію про хімічний елемент з порядковим номером 7, одержану вами з періодичної системи хімічних елементів.
5. Розташуйте хімічні елементи за збільшенням заряду ядра атома:
А Сульфур;
Б Нітроген;
В Ферум;
Г Карбон.
6. Розташуйте хімічні елементи за збільшенням кількості електронів в атомі:
А Фосфор;
Б Гідроген;
В Хлор;
Г Кальцій.
7. Розташуйте хімічні елементи за зменшенням відносної атомної маси:
А Калій;
Б Алюміній;
В Цинк;
Г Силіцій.
8. Поясніть, чому у більшості хімічних елементів періодичної системи відносна атомна маса виражена дробовими числами.
9. Користуючись текстом параграфа, поясніть, який різновид атомів Гідрогену з Аr = 1, чи з Аr = 2 переважає у природі.
10. Заповніть таблицю інформацією, якої не вистачає:
Назва Елемента | Символ | Аr | Склад атома |
Кількість протонів | Кількість нейтронів | Кількість електронів | |
Оксиген | |||
S | |||
40 | |||
47 | |||
13 |
11. Дізнайтеся з додаткових джерел інформації про походження назв хімічних елементів, підготуйтесь до презентації результатів своєї пошукової діяльності.
Потренуйтеся у використанні періодичної системи як довідкової. Для цього вдома підготуйте 2-3 запитання, щоб задати учням своєї малої навчальної групи.
