Природні джерела і застосування вуглеводнів – АРОМАТИЧНІ ВУГЛЕВОДНІ (АРЕНИ)
Хімія підготовка до ЗНО та ДПА
Комплексне видання
ЧАСТИНА І
ЗАГАЛЬНА ХІМІЯ
ОРГАНІЧНА ХІМІЯ
АРОМАТИЧНІ ВУГЛЕВОДНІ (АРЕНИ)
Природні джерела і застосування вуглеводнів
Перегонка нафти
Багато органічних речовин, з якими ви маєте справу в повсякденному житті,- пластмаси, фарби, мийні засоби, ліки, лаки, розчинники – синтезовані з вуглеводнів. У природі є три основних джерела вуглеводнів – нафта, природний газ і кам’яне вугілля.
Нафта – одне з найважливіших корисних копалин. Сучасне суспільство неможливо
Нафта – темна масляниста рідина, що залягає в земній корі на різній глибині. Вона являє собою однорідну суміш складного виду, в якій міститься кілька сотень речовин – переважно насичених вуглеводнів з числом атомів Карбону від 1 до 40. При переробці цієї суміші викорітстовують як фізичні, так і хімічні методи.
Спочатку нафту розділяють на простіші суміші (фракції) шляхом перегонки, заснованої на тому, що різні речовини у складі нафти киплять при різних температурах.
Функції
Фракція | Число атомів Карбону в молекулах | Температура кипіння, С | Застосування |
Газова фракція | 1-4 | < 20 °С | Паливо |
Бензин | 5-10 | 20-180 °С | Автомобільне паливо |
Лігроїн | 6-12 | 160-200 °С | Паливо, сировина для синтезу |
Гас | 10-16 | 180-250 °С | Авіаційний бензин |
Газойль | 13-25 | 220-350 °С | Дизельне паливо |
Важкий газойль (мазут) | 26-30 | 350-430 °С | Паливо для теплоелектростанцій |
Важкий мазут | > 30 | При нагріванні розкладається, переганяють під вакуумом | Виробництво асфальту, мастильних матеріалів, паливо для котелень |
Перегонка відбувається в ректифікаційній колоні при сильному нагріванні. Найважчі фракції, що за високої температури розкладаються, переганяють за зниженого тиску.
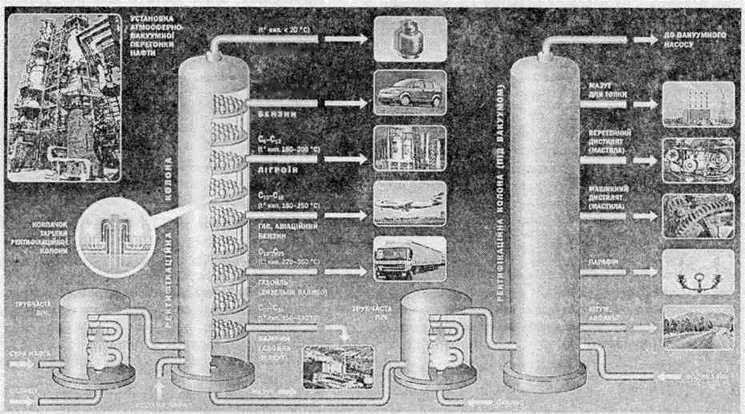
Хімічна переробка нафтопродуктів
Багато продуктів перегонки нафти можна застосовувати відразу, без подальшої переробки. Однак найбільшу цінність для промисловості представляють легкі фракції – бензин і гас, але вихід їх при перегонці невеликий. До того ж після перегонки виходить бензин низької якості (з невеликим октановим числом), тому що нафта в основному містить вуглеводні з нєрозгалуженим карбоновим кістяком, які при стискуванні детонують. Двигун, що працює на такому паливі, видає характерний стукіт і швидко виходить із ладу. Для підвищення якості бензину і збільшення його виходу нафту піддають хімічній переробці.
Один з найважливіших способів хімічної переробки нафти – крекінг. При нагріванні до 500 °С без доступу повітря у присутності спеціальних каталізаторів довгі молекули алканів розщеплюються на дрібніші. Під час крекінгу з насичених вуглеводнів утворюється суміш легших насичених і ненасичених вуглеводнів, наприклад:

Цей процес приводить до збільшення виходу бензину і гасу. Якщо крекінг проводити в присутності алюмосилікатних каталізаторів (каталітичний крекінг), то утворюються алкани переважно розгалуженої будови, що підвищує якість палива (крекінг-бензин).
За сильнішого нагрізання нафти (до 700-900 °С) розщеплюються навіть молекули середніх розмірів, наприклад:

У суміші залишаються тільки найпростіші вуглеводні, переважно ненасичені. Цей процес, що називають піролізом, проводять для добування етилену – вихідної речовини для синтезу етанолу і пластмас. При піролізі утворюються також ароматичні вуглеводні.
Основоположником сучасних методів переробки нафти є видатний хімік В. М. Іпатьєв.
Однією з характеристик, якою позначають якість бензину, є так зване октанове число, що показує можливість детонації паливно-повітряної суміші в двигуні. Розглянемо, як впливає детонація на роботу двигуна. В циліндр двигуна внутрішнього згоряння подається суміш парів бензину з повітрям. При нормальній роботі двигуна в циліндрі ця суміш стискується поршнем і підпалюється свічкою:
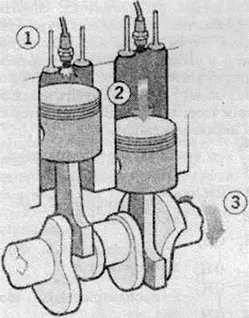
Схема роботи двигуна внутрішнього згоряння:
1 – паливно-повітряна суміш стискується поршнем і підпалюється;
2 – продукти згоряння займають більший об’єм, тому витискують поршень;
3 – поршень прокручує вал двигуна.
Оскільки продукти згоряння мають більший об’єм, ніж вихідна суміш, вони штовхають назад поршень, який прогсручає колінвал. Але бензин низької якості не встигає підпалитися свічкою, а при стисканні поршнем вибухає (детонує), і сила, що вивільнюється, не використовується на роботу двигуна. Це призводить до руйнування двигуна і погіршення його роботи. Чим вище значення октанового числа, тим менше вірогідність детонації бензину, а отже вище його якість.
Нормальний гептан – абсолютно непридатний як моторне паливо, він детонує майже завжди. В той же час 2,2,4-триметилпентан (ізооктан) має унікальні властивості: він майже не детонує у двигуні. Ці дві речовини лежать в основі шкали вимірювання якості бензину – шкала октанових чисел. В цій шкалі гептану присвоєно значення нуль, а ізооктанові – сто. Згідно з цією шкалою бензин з октановим числом 90 має такі самі детонаційні властивості, як і суміш 90% ізооктану і 10% гептану.
Природний газ
Друге за важливістю джерело вуглеводневої сировини – природний газ, головною складовою частиною якого є метан. Природний газ використовують у першу чергу як ефективне паливо. При його згорянні не утворюється ані зола, ані отрутний чадний газ, тому природний газ вважають екологічно чистим паливом. Велику кількість природного газу використовує хімічна про мисловість.
Його переробка зводиться головним чином до одержання ненасичених вуглеводнів і синтезу-газу. Етилен і ацетилен утворюються при відщепленні водню від нижчих алканів, а синтез-газ – суміш карбон(ІІ) оксиду і водню – одержують нагріванням метану з водяною парою:
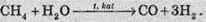
Із цієї суміші, застосовуючи різні каталізатори, синтезують оксигеновмісні сполуки – метиловий спирт, оцтову кислоту тощо.
Просуваючись над кобальтовим каталізатором, синтез-газ перетворюється в суміш алканів, що являє собою синтетичний бензин:

Кам’яне вугілля
Ще одне джерело вуглеводнів – кам’яне вугілля. У хімічній промисловості його переробляють шляхом коксування – нагрівання до 1000 °С без доступу повітря. При цьому утворюються кокс і кам’яновугільна смола, маса якої становить усього кілька відсотків від маси вугілля. Кокс використовують як відновник в металургії (наприклад, для добування заліза з його оксидів).p>
Кам’яновугільна смола містить кілька сотень органічних сполук, в першу чергу – ароматичних вуглеводнів, які виділяють з неї перегонкою.
Кам’яне вугілля також використовують як паливо, однак при цьому виникають серйозні екологічні проблеми. По-перше, вугілля містить негорючі домішки, які при окисненні палива перетворюються в шлаки; по-друге, у складі вугілля є невеликі кількості сполук Сульфуру і Нітрогену, при згорянні вони утворюють оксиди, що забруднюють атмосферу.