Силіцій – Елементи IV групи
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ
9. Неметалічні елементи та їхні сполуки. Неметали
9.5. Елементи IV Групи
9.5.6. Силіцій
Силіцій – 14-й елемент періодичної таблиці, заряд ядра – +14. Хімічний символ – Si, відносна атомна маса – 28. Відомо три стабільні природні ізотопи Силіцію: 28Si (92,27 %), 29Si, 30Si. Утворює просту речовину кремній. Електронна формула – 14Si 1s22s22p63s23p2; валентність – II (основний стан), IV (збуджений стан).
Виявляє ступені окиснення -4, 0, +2, +4. Існує невелика
Ступінь окиснення | -4 | 0 | +4 |
Приклади сполук | SiH4, Mg2Si | Si | SiO2, H2SiO3 |
Поширеність Силіцію в природі
Силіцій – один з найпоширеніших елементів (27,6 % маси) земної кори, посідає друге місце за поширеністю після Оксигену. Концентрація у воді (і морській, і прісній) – 3 мг/л.
Найчастіше в природі Силіцій трапляється
Стікати – велика група (близько 800) складних мінералів на основі сполук Силіцію й Оксигену. Якщо до складу природного силікату входить ще й алюміній оксид Аl2O3, то їх називають алюмосилікатами (до 50 % маси земної кори). Це біла глина Al2O3 · 2SiO2 · 2Н2O, польові шпати (К, Na, Са)O2 · Аl2O3 · SiO2 (з яких на 60-65 % складається граніт), слюда К2O · Аl2O3 · 6SiO2 · Н2O. Силікати разом з алюмосилікатами становлять близько 90% мінералів літосфери. Деякі природні силікати є дорогоцінними каменями: аквамарин, топаз, смарагд, нефрит, родоніт, турмалін, берил, гранат.
Гірські породи, що лежать на поверхні, із часом вивітрюються, тобто руйнуються за участі атмосферних, біологічних чинників і води. Розрізняють вивітрювання фізичне (механічне, внаслідок дії вітру і заморожування-розморожування води), біологічне і хімічне. Ось приклад хімічного вивітрювання:
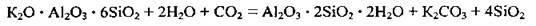
Унаслідок вивітрювання утворюються поклади глини, піску та солей. Зрідка трапляється самородний кремній. У живій природі Силіцію не дуже багато. Його накопичують деякі рослини: злаки (оболонка зерна, стебло: що воно твердіше, то більше там Силіцію), польовий хвощ, бамбук, очерет, деякі водорості. Він основа скелетів деяких морських організмів – радіолярій, діатомей, губок, морських зірок. В організмі людини він міститься у незначній кількості (близько 1 г), головним чином у кістках, нігтях та волоссі, але при переломах кісток його концентрація в місці перелому зростає майже в 50 разів.
Фізичні властивості простих речовин Силіцію
Силіцій утворює дві прості речовини, тобто дві алотропічні видозміни: силіцій кристалічний та аморфний (насправді це тонко-дисперсний порошок з кристалічного кремнію).
Кристалічний кремній має алмазоподібні кристалічні гратки. Однак зв’язки між атомами Силіцію є набагато слабшими, ніж зв’язки між атомами Карбону в алмазі. За стандартних умов частина зв’язків руйнується і з’являються вільні електрони, які зумовлюють незначну електропровідність. Кристалічний кремній має темно-сірий колір і металічний блиск, твердий, але крихкий, напівпровідник. Його електропровідність зростає при освітленні та нагріванні.
Аморфний кремній – це бурий порошок, більш хімічно активний, ніж кристалічний. Не розчиняється в жодному розчиннику.
Добування кремнію
У лабораторії проводять реакцію між чистим кварцовим піском і магнієм:
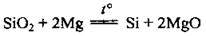
У промисловості силіцій добувають з піску і коксу в електропечах за температури 1800 °С:
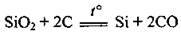
Хімічні властивості кремнію
Силіцій – неметал з невисокою хімічною активністю. Його неметалічні властивості менше виражені порівняно з вуглецем. Аморфний силіцій значно активніший за кристалічний. Хімічна активність кристалічного силіцію зростає при нагріванні. Усі реакції, характерні для силіцію, є окисно-відновними. Більш характерні є відновні властивості.
Взаємодія з простими речовинами. За стандартних умов кремній реагує лише із фтором, а при нагріванні сполучається з іншими галогенами, киснем, сіркою, азотом, вуглецем:
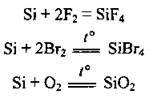
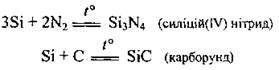
Окислювальні властивості силіцію виявляються в реакціях з металами:
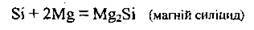
Силіциди легко розкладаються кислотами і водою:
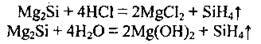
Силан SiH4 – газ, що самозапалюється на повітрі:
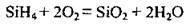
Взаємодія зі складними речовинами. З кислотами силіцій не реагує. Силіцій реагує з розчинами лугів, виділяючи водень:
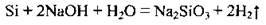
Застосування кремнію
Кремній як напівпровідник використовують у мікроелектроніці, обчислювальній техніці. Це сировина для металургії (виплавляння чавуну, бронзи, силуміну); кремній уводять до складу сплавів, для яких характерна здатність до швидкого намагнічування і розмагнічування (виготовлення трансформаторів); сталі із вмістом Силіцію 20 % є кислотостійкими (виготовлення хімічної апаратури). Кремній також використовують для виготовлення фотоелементів, сонячних батарей. Із кремнію добувають карборунд, завдяки його великій твердості (9-9;5 за шкалою Мооса) його використовують як абразивний матеріал, у виробництві композитних матеріалів, ювелірних виробів тощо. Силіцій застосовують у виробництві кремнійорганічних сполук, які, у свою чергу, є сировиною для виготовлення мастил, полімерів, гум, каучуків (з температурним інтервалом від -80 до +260 °С), кремнійорганічних рідин та емульсій.