Хімічні властивості кисню: реакції з простими речовинами. Оксиди
Розділ 2 Кисень
21 Хімічні властивості кисню: реакції з простими речовинами. Оксиди
Матеріал параграфа допоможе вам:
> оцінити здатність кисню вступати в реакції з металами і неметалами;
> з’ясувати, що таке реакція сполучення і які сполуки називають оксидами;
> навчитися складати формули оксидів і називати ці сполуки.
Хімічні властивості кожної речовини виявляються в хімічних реакціях за її участю.
Кисень – один із найактивніших неметалів. Але за звичайних умов він реагує з небагатьма речовинами. Його
Реакції кисню з простими речовинами. Кисень взаємодіє (як правило – при нагріванні) з більшістю неметалів і майже з усіма металами.
Реакція з вуглецем (вугіллям). Відомо, що вугілля, нагріте па повітрі до високої температури, загоряється. Це свідчить про перебіг хімічної реакції речовини з киснем.
Основним продуктом згоряння вугілля є вуглекислий газ СО2. Вугілля – суміш багатьох речовин. Масова частка Карбону в ньому перевищує 80 %. Вважаючи, що вугілля складається лише з атомів Карбону, напишемо відповідне хімічне рівняння:
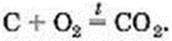
Вуглекислий газ може містити домішку чадного газу – продукту іншої реакції:
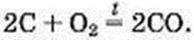
Прості речовини Карбону графіт і алмаз (їх узагальнена хімічна назва – вуглець) взаємодіють із киснем так само, як і вугілля.
Реакцію, в якій беруть участь кілька речовин, а утворюється одна, називають реакцією сполучення.
Реакція з воднем. Якщо газ водень, що утворюється під час відповідної реакції в пробірці й виходить у повітря через тонку газовідвідну трубку, підпалити, то він горітиме ледь помітним полум’ям. Єдиним продуктом такої реакції є вода. Це можна довести, помістивши над полум’ям скляну пластинку. На пій з’являтимуться краплинки води внаслідок конденсації водяної пари.
► Складіть рівняння реакції горіння водню.
Суміш водню з повітрям або киснем при підпалюванні вибухає.
Реакція із сіркою. Таке хімічне перетворення здійснює кожний, коли запалює сірник; сірка входить до складу голівки сірника. У лабораторії реакцію кисню із сіркою проводять у витяжній шафі. Невелику кількість сірки (мал. 61, а) нагрівають у залізній ложці. Речовина спочатку плавиться, а потім загоряється внаслідок взаємодії з киснем повітря і горить ледь помітним блакитним полум’ям (мал. 61, б). З’являється різкий запах продукту реакції – сірчистого газу (цей запах ми відчуваємо в момент загоряння сірника). Хімічна формула сірчистого газу – SО2, а рівняння реакції –
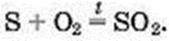
Якщо ложку із сіркою, що горить, помістити в посудину з киснем, то сірка горітиме яскравішим полум’ям (мал. 61, в), ніж на повітрі. Це й зрозуміло, бо чистий кисень, на відміну від повітря, містить лише молекули О2.

Мал. 61. Сірка (а) та її горіння на повітрі (б) й у кисні (в)
Реакція з магнієм. Раніше цю реакцію використовували фотографи для створення миттєвого потужного освітлення (“магнієвий спалах”) під час фотозйомки. У хімічній лабораторії відповідний дослід проводять так. Металевим пінцетом беруть магнієву стрічку і підпалюють на повітрі. Магній горить сліпучо-білим полум’ям (мал. 62). Внаслідок реакції утворюється біла тверда речовина – сполука Магнію з Оксигеном.
► Складіть рівняння реакції магнію з киснем.

Мал. 62. Магній (а) та його горіння на повітрі (б)
Реакція із залізом. Сильно розігріте залізо в чистому кисні горить. Дослід зі спалювання леза або сталевої пружинки є дуже ефектним. На пружинці закріплюють сірник (мал. 63). Потім пружинку затискують у лабораторних щипцях. Сірник спрямовують голівкою донизу і підпалюють. Коли полум’я досягне пружинки, її відразу переносять у склянку з киснем. Дно посудини заздалегідь засипають шаром піску, щоб на скло не потрапили краплі розплавленого металу. Пружинка згоряє в кисні, розкидаючи іскри на всі боки (це нагадує процес зварювання металу):
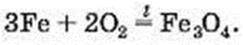

Мал. 63. Горіння сталевої пружинки в кисні
Формулу продукту реакції можна записати й так: FeO ∙ Fe2О3. Крапка між двома хімічними формулами означає, що це не суміш сполук Феруму, а одна, індивідуальна сполука. Її поширена назва – залізна окалина.
Реакція з міддю. Якщо нагрівати на повітрі мідну дротинку або пластинку з очищеною до блиску поверхнею, то побачимо поступову зміну її темно-червоного (“мідного”) кольору на темно-сірий. Такий колір мас плівка сполуки Купруму з Оксигеном, що утворюється на металі внаслідок реакції
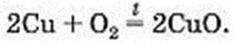
Оксиди. Продуктами всіх реакцій, розглянутих у параграфі, є бінарні сполуки елементів з Оксигеном.
Сполуку, утворену двома елементами, одним із яких є Оксиген, називають оксидом.
Склад майже всіх оксидів відповідає загальній формулі ЕmОn, у якій індекс т може набувати значень 1 або 2.
Кожний оксид має хімічну назву, а деякі – ще й традиційні, або тривіальні1, назви (табл. 3). Хімічна назва оксиду складається із двох слів. Першим словом є назва відповідного елемента, а другим – слово “оксид”. Якщо елемент має змінну валентність, то він може утворювати кілька оксидів. Зрозуміло, що їхні назви мають відрізнятися. Для цього після назви елемента вказують (без відступу) римською цифрою в дужках значення його валентності в оксиді. Приклад такої назви сполуки: хром() оксид (читається “хром-три-оксид”).
Таблиця 3
Формули і назви деяких оксидів
Формула | Назва | |
Традиційна (тривіальна) | Хімічна | |
СО2 | Вуглекислий газ | Kap6oн(IV) оксид |
СО | Чадний газ | Карбон(ІІ) оксид |
СаО | Негашене вапно | Кальцій оксид |
У хімічних назвах оксидів відмінюється лише друге слово: магній оксиду, ферум(ІІІ) оксидом.
Якщо елемент виявляє змінну валентність, то оксид, у якому значення валентності цього елемента є для нього максимальним, називають вищим. Вищий оксид Карбону – сполука з формулою СО2.
ВИСНОВКИ
Кисень – хімічно активна речовина. Він взаємодіє з більшістю простих речовин. Продуктами таких реакцій є сполуки елементів з Оксигеном – оксиди.
Реакції, внаслідок яких із кількох речовин утворюється одна, називають реакціями сполучення.
1 Слово походить від латинського trivialis – звичайний.
?
156. Чим різняться реакції сполучення і розкладу?
157. Виберіть серед наведених формул ті, що відповідають оксидам: О2?
NaOH, Н2О, НСl, l2O5, ВаО.
158. Встановіть відповідність:
Формула оксиду
1) FeO;
2) Fe2O3;
3) Fe3O4;
Назва оксиду
А) ферум(ІІІ) оксид;
Б) ферум(ІІ, III) оксид;
В) ферум(ІІ) оксид.
159. Дайте хімічні назви оксидам із такими формулами: NO, Ті2O3, Сu2O, Сl2O7, V2O5, СrO3. Зважте на те. що елементи, які утворюють ці оксиди, мають змінну валентність.
160. Запишіть формули плюмбум(ІV) оксиду, хром(ІІІ) оксиду, хлор(І) оксиду, осмій(VІІІ) оксиду.
161. Допишіть формули простих речовин у схемах реакцій і складіть хімічні рівняння:
А) NO; в) … + … -> Аl2O3;
Б)… + … -> СаО; г)… + … -> Li2O.
162. Назвіть усі можливі значення індексу n у загальній формулі оксидів ЕmOn, якщо: а) m = 1; б) m = 2.
163. Обчисліть масову частку Оксигену в бор оксиді.
164. Дві колби заповнили киснем. В одній колбі спалили магній, узятий в надлишку, а в іншій – надлишок сірки. Під час горіння речовин посудини були герметично закриті. У якій колбі утворився вакуум? Відповідь поясніть.
