Корозія металів – Загальні відомості про металічні елементи та метали
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ
8. Металічні елементи та їхні сполуки. Метали
8.1. Загальні відомості про металічні елементи та метали
8.1.4. Корозія Металів
Корозія (від лат. corrosio – роз’їдання) – це самовільний процес руйнування металів при взаємодії з навколишнім середовищем. Розрізняють кілька видів корозії, з яких найважливішими є хімічна й електрохімічна.
Хімічна корозія
Цей вид корозії спричинений взаємодією металів з корозійно-активним
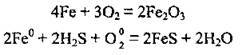
Більшість металів окислюється киснем повітря, утворюючи на поверхні оксидні плівки, які захищають ці метали від подальшої корозії1:
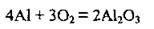
Такі щільні захисні плівки утворює алюміній, хром, цинк,
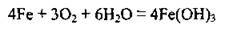
Швидкість хімічної корозії залежить від температури, црироди навколишнього середовища, активності металу, його чистоти (надчисте залізо практично корозії не піддається2). З підвищенням температури” зазвичай, інтенсивність корозії зростає. Це зумовлюється швидкістю дифузії, зокрема кисню і металу крізь оксидну плівку на поверхні металу, та утворенням тріщин, крізь які кисень проникає глибше в метал і окислює його.
За наявності деяких речовин, які руйнують захисну оксидну плівку, корозія відбувається особливо енергійно. Речовини, що пришвидшують корозію металів і сплавів, називають активаторами корозії. До енергійних активаторів належать розчинений у воді кисень, хлорид-йони Сl-. Саме йони Сl-, яких багато в морській воді, сприяють активній корозії підводних частин кораблів.
Електрохімічна корозія
Електрохімічна корозія відбувається при контакті металевих виробів з двох різних металів (з різними окисно-відновними потенціалами) у корозійному середовищі й супроводжується виникненням електричного струму. При контакті двох металів, наприклад цинку й міді, утворюється гальванічний елемент: відбувається процес окиснення цинку як активнішого металу і перехід катіонів Zn2+ у шар електроліту. Вільні електрони приєднують йони Гідрогену Н+:
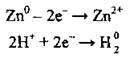
Крім окиснення активнішого металу, спостерігається перенесення електронів від активнішого металу до менш активного – виникає струм. Такі електрохімічні процеси відбуваються завжди при контакті двох різних металів у розчині електроліту. При цьому більш активний метал завжди руйнується.
Корозійним середовищем може бути розчин електроліту, грунтова вода, вода природних водойм (особливо морська), звичайна дощова вода або конденсат (сконденсована волога повітря), у яких завжди розчинена якась кількість вуглекислого газу.
Захист металів від корозії
Виділяють три основні напрямки захисту від корозії: конструкційний, активний і пасивний.
1. Конструкційний напрямок передбачає використання конструкційних матеріалів, які виготовлені з корозійностійких матеріалів – нержавіючих3, легованих4 сталей, кольорових металів та їхніх сплавів, інших матеріалів (кераміки, пластмаси), стійких до негативного впливу навколишнього середовища, а також застосування клеїв, герметиків, прокладок тощо.
2. Активний захист передбачає використання двох основних методів електрохімічного захисту: протекторного і катодного:
А) протекторний: до підземних трубопроводів, корпусів суден та різних металевих конструкцій, які постійно перебувають у корозійному середовищі, під’єднують “жертовний анод” з активнішого металу (магнію, цинку), що руйнується в першу чергу;
Б) катодний: металоконструкцію під’єднують до катода зовнішнього джерела струму, що підвищує електродний потенціал металу і запобігає корозії.
Також для зменшення корозії корозійне середовище піддають спеціальній обробці:
– введення інгібіторів, які сповільнюють процес корозії (сьогодні відомо понад 5 тисяч таких інгібіторів);
– видалення розчиненого у воді повітря (деаерація), наприклад води, яка надходить до котельних установок.
3. Найпоширенішим способом захисту металу від корозії є пасивний – покриття захисним шаром5. Розрізняють неметалічні, металічні та хімічні покриття:
А) неметалічні покриття: спеціальні лаки, фарби, емалі, каучуки (гумування);
Б) металічні покриття – осадження одного металу для захисту певної деталі, виготовленої з іншого металу чи сплаву, проводять:
– хромування, нікелювання електролітичним методом (гальванізація);
– методами холодного, гарячого і термодифузійного цинкування6;
– методом газотермічного напилення;
– методом лудіння7;
В) до хімічних відносять штучні покриття – поверхневі плівки (оксидні, фосфатні, нітридні тощо), їх наносять на поверхню металу, і процес корозії гальмується.
Слід зазначити, що захисту від корозії піддають конструкції, виготовлені не лише із заліза, а й з інших Металів, наприклад з алюмінію, оксидну плівку якого підсилюють анодним окисненням (анодуванням).
Незважаючи на успіхи у боротьбі з корозією, проблема постійно загострюється через збільшення металевого фонду, ускладнення умов експлуатації металоконструкцій, а саме: використання високо агресивних середовищ (хімічна промисловість, ядерна та геотермальна галузі енергетики, розробка шельфу тощо), підвищення робочих температур, тиску і швидкостей потоків, забруднення атмосфери SО2 та іншими газами, застосування металевих конструкцій під напруженням (корозія під напруженням). Сумарні збитки від корозії та затрати на захист від неї у промислово розвинених країнах сягають 4 % національного доходу і більше.
_______________________________________________________________
1 Пасивація металів – перехід поверхні металу в неактивний (пасивний) стан, пов’язаний з утворенням тонких поверхневих шарів сполук, що запобігають подальшому протіканню реакції (корозії).
2 Інколи кородувати можуть і надчисті метали. Зазвичай це зумовлено дефектами в кристалах металу, подряпинами його поверхні, тому якісна механічна обробка металу гальмує передчасну корозію.
3 Вміст хрому в нержавіючій сталі – не менше 12 %.
4 Пасиваційна плівка таких сталей є не пухкою, а щільною.
5 На 80 % захист від корозії забезпечують правильною підготовкою поверхні металевого виробу (очистка від окалини, іржі, залишків старої фарби тощо) і лише на 20 % -; власне покриттям (матеріал, якість, спосіб).
6 На це витрачають до 40 % добутого у світі цинку.
7 Гаряче лудіння (покриття оловом) – найдавніший спосіб захисту металів від корозії. Його використовували ще у V ст. до н. е. Луджені листи сталі 0,08-0,32 мм завтовшки називають білою бляхою. їх в основному застосовують для виготовлення консервних бляшанок.
