Мило – ЕСТЕРИ, ЖИРИ ТА МИЛО
Хімія підготовка до ЗНО та ДПА
Комплексне видання
ЧАСТИНА І
ЗАГАЛЬНА ХІМІЯ
ОРГАНІЧНА ХІМІЯ
ЕСТЕРИ, ЖИРИ ТА МИЛО
Мило
Милом є солі вищих карбонових кислот. Як і жири, мило можна класифікувати за агрегатним станом у звичайних умовах. Так, розрізняють тверде мило (натрієві солі вищих карбонових кислот) і рідке мило (калієві солі вищих карбонових кислот). Відповідно, формула мила: С17Н35СООNа – натрій стеарат та С17Н35СООК – калій стеарат.
Основний метод добування мила – гідроліз жирів. Якщо жир нагрівати з розчином
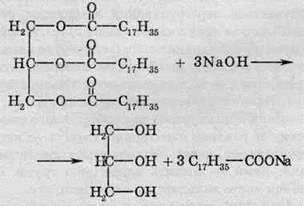
Виробництво мила вимагає великої витрати жирів. Тим часом жири – найцінніший продукт харчування. Щоб зберегти їх, мило краще добувати з нехарчової сировини. Сьогодні такі можливості надає органічна хімія.
До складу мила входять солі вищих карбонових кислот. Зараз такі кислоти добувають у промисловості окисненням вуглеводнів, що входять
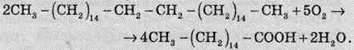
У результаті утворюється суміш різних кислот та інших оксигеновмісних сполук, які піддають роз’єднанню.
Нейтралізацією кислот добувають солі. Ці солі (у суміші з наповнювачем) ідуть на виробництво туалетного та господарського мила. Але мило, добуте із синтетичних кислот, аналогічне за своєю хімічною природою до звичайного мила, отже, має його недоліки: погано миє у твердій воді. Саме тому зараз розвивається виробництво мийних засобів іншого типу: це синтетичні мийні засоби (СМЗ), Один із видів СМЗ являє собою сіль кислих естерів вищих спиртів та сульфатної кислоти:
Схема добування (у загальному вигляді):
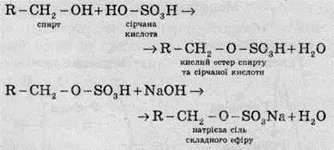
Дуже розповсюдженим видом є алкілбензосульфонати:
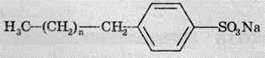
За будовою такі солі подібні до солей, що входять до складу звичайного мила (вони, як і мило, мають поверхневу активність і гарну мийну дію). Але, на відміну від звичайного мила, такі речовини не втрачають мийних властивостей у твердій воді, тому що утворені при цьому кальцієві та магнієві солі виявляються розчинними й, отже, поверхнево-активна речовина залишається у воді, а не випадає в осад.