Приклади розв’язування типових задач – Урок 3
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ І. ЗАГАЛЬНА ХІМІЯ
3. Хімічний зв’язок
Приклади розв’язування типових задач
Задача 1. Укажіть кількість р-електронів, які утворюють хімічні зв’язки у молекулі хлор(І) оксиду.
Розв’язання
Сl2O. Будова електронних оболонок елементів Хлору і Оксигену:

З формули видно, що Хлор перебуває в основному (незбудженому) стані та виявляє валентність І. При утворенні молекули оксиду відбувається перекриття р-орбіталей
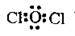
Отже, кількість р-електронів, які утворюють хімічні зв’язки у молекулі хлор(І) оксиду, дорівнює чотирьом.
Задача 2. Укажіть кількість електронів, які беруть участь в утворенні хімічних зв’язків у молекулі 1,2-дихлоретену.
Розв’язання
Структурна формула речовини:
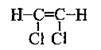
З формули видно, що у молекулі є 6 спільних пар електронів. Отже, кількість електронів, які утворюють хімічні зв’язки у молекулі 1,2-дихлоретену, дорівнює 12.
Задача 3. Укажіть неметалічні елементи, між атомами яких утворення
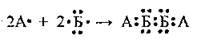
Розв’язання
Елемент А у зовнішньому електронному шарі містить лише 1 електрон – це Гідроген. Елемент Б у зовнішньому електронному шарі містить 6 електронів – це Оксиген. Отже, це речовина гідроген пероксид.
Задача 4. Укажіть тип зв’язку для речовини, які утворена елементами з порядковими номерами 20 і 9.
Розв’язання
Елемент з порядковим номером 20 – Кальцій – типовий металічний елемент, лужноземельний. Елемент з порядковим номером 9 – Флуор – типовий неметалічний елемент, галоген. При їх сполученні утворюється речовина з іонним типом зв’язку.
Задача 5. Елемент А з конфігурацією зовнішнього електронного шару 2s22р4 утворює ковалентну сполуку з Гідрогеном і елементом Б з конфігурацією зовнішнього електронного шару 2s22р2 у його збудженому стані. Складіть електронну формулу сполуки та вкажіть загальну кількість електронів, які взяли участь в утворенні зв’язків.
Розв’язання
Елемент А 2s22р4 – Нітроген, елемент Б 2s22р2 – Карбон. Електронна оболонка Карбону у збудженому стані – 2s12р3. Електронна формула сполуки, яка утворилась:
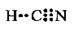
В утворенні зв’язку взяло участь 8 електронів.
Задача 6. Із запропонованого ряду формул речовин: СО2, SО2, SiО2, LiOH, HF, CuO, C3H8, C6H12О6 виберіть такі, що мають молекулярні кристалічні гратки. Укажіть суму молярних мас цих речовин.
Розв’язання
Молекулярні кристалічні гратки серед наведеного ряду речовин мають:
– карбон(ІV) оксид, СO2 – газ (за н. у.), М(СO2) = 44 г/моль;
– сульфур(ІV) оксид, SO2 – газ, M(SO2) = 64 г/моль;
– пропан, С3Н8 – газ, М(С3Н8) = 44 г/моль;
– глюкоза, С6Н12O6 – тверда речовина, М(С6Н12О6) = 180 г/моль.
Сума їхніх молярних мас становить 332 г/моль.