Реакції обміну між розчинами електролітів, умови їх протікання
Тема 1
РОЗЧИНИ
УРОК 14
Тема уроку. Реакції обміну між розчинами електролітів, умови їх протікання
Цілі уроку: показати процеси, що протікають у розчинах електролітів як реакції обміну між іонами; ознайомити з умовами їх протікання; формувати навички складання іонних рівнянь.
Тип уроку: формування вмінь і навичок та їх творчого застосування.
Форми роботи: розповідь учителя, демонстраційний експеримент, виконання тренувальних вправ.
Обладнання: таблиця розчинності, набір реактивів, лабораторне устаткування. Демонстрація
ХІД УРОКУ
I. Організація класу
II. Перевірка домашнього завдання.
Актуалізація опорних знань
1. Двоє учнів працюють біля дошки, решта – у зошитах виконують завдання.
Напишіть рівняння дисоціації запропонованих речовин.
Na2SО4
Na2CО3
Ва(ОН)2
Ca(ОH)2
HCl
LiОH
K2CО3
K3PО4
H3PО4
H2SО4
2. Фронтальне опитування (по ланцюжку)
Продовжте визначення.
Електроліти – це…
Ступінь дисоціації – це…
Кислота – це…
Основа – це…
Сіль – це…
Електролітична дисоціація – це…
ІІІ. Сприйняття
Демонстрація 4
Згадайте, які явища супроводжують хімічні реакції.
Ми з’ясували, що в розчині електроліти перебувають у формі іонів.
Дослід 1
Візьмемо два розчини: BaSО4 і Na2SО4.
Запишіть рівняння дисоціації цих солей:
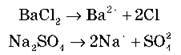
Змішуємо розчини. Що відбувається? Осад BaSО4 свідчить про протікання хімічної реакції.
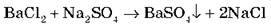
Оскільки в розчині BaCl2, Na2SО4 і NaCl перебувають у вигляді іонів, запишіть рівняння в іонній формі.
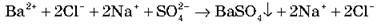
Розчинність BaSО4 настільки мала, що більша частина його в розчині перебуває у вигляді молекул BaSО4.
Отже, у розчині протікає реакція зв’язування іонів Ba2+ і SО24-, що описується рівнянням:
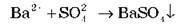
Дослід 2
Для наступної реакції візьмемо розчин натрій гідроксиду (з фенолфталеїном) і додамо по краплях хлоридну кислоту до зникнення малинового забарвлення. Ознака реакції – зникнення забарвлення індикатора:
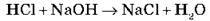
НCl, NaОН, NaCl – сильні електроліти, тобто в розчині перебувають у вигляді іонів.
Тоді запишемо рівняння реакції в іонній формі:
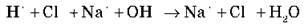
H2O – слабкий електроліт, ступінь дисоціації дорівнює 1,4 – 10-9. Тому практично протікає реакція:
H++ OH – 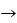 H2O
H2O
Дослід 3
До розчину Na2CO3 додамо розчин хлоридної кислоти. Ознака реакції – виділення вуглекислого газу:
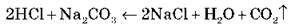
НО, Na2CО3, NaCl – сильні електроліти, тому в розчині перебувають у вигляді іонів.
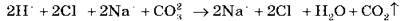
H2О і CО2 – слабкі електроліти, тому суть процесу описує рівняння:
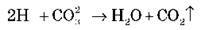
Отже, виділяють три умови незворотного протікання реакцій:
– утворення нерозчинної або малорозчинної речовини;
– утворення газоподібної речовини;
– утворення речовини, що дисоціює незначною мірою, наприклад H2О.
IV. Керована практика
Самостійна робота під керівництвом учителя.
Завдання 1
Запишіть рівняння в молекулярній повній та скороченій іонній формах.
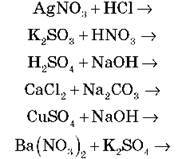
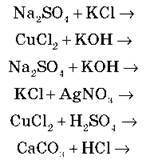
Завдання 2
Виберіть рівняння можливих реакцій.
V. Підбиття підсумків уроку, виставлення оцінок
VI. Домашнє завдання
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
За таблицею розчинності підібрати три-чотири пари речовин, між якими можна записати іонні рівняння.