Загальна характеристика – Урок 3 – Елементи VIA групи
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ
9. Неметалічні елементи та їхні сполуки. Неметали
9.3. Елементи VIA Групи
9.3.1. Загальна характеристика
До складу головної підгрупи VI групи1 належать Оксиген, Сульфур, Селен, Телур і Полоній. Елементи цієї підгрупи ще називають халькогенами2, або елементами підгрупи Оксигену.
Це p-елементи; будова зовнішнього електронного рівня халькогенів – ns2np4, де n – номер періоду.
Валентність елементів буває II, IV та VI, а в Оксигену
До завершення зовнішнього електронного шару халькогенам не вистачає двох електронів, а тому їхні атоми легко приєднують електрони, утворюючи йон Е2-, який є в йонних сполуках. У ковалентних сполуках, де халькоген є електронегативнішим елементом, він виявляє також найнижчий ступінь окиснення (-2). У сполуках з електронегативнішими неметалічними елементами всі халькогени (крім Оксигену) виявляють ступені окиснення +6 або +4.
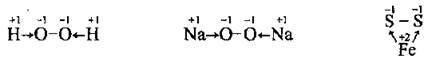
Оксиген виявляє позитивний ступінь окиснення +2 лише в сполуці з електронегативнішим Флуором OF2:
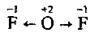
Сполуки елементів підгрупи Оксигену зі ступенем окиснення халькогену -2 виявляють відновні властивості, які посилюються закономірно зі зменшенням електронегативності в ряду від Сульфуру до Телуру.
У підгрупі зверху донизу зі збільшенням заряду ядра атома збільшуються атомні радіуси елементів і зменшується електронегативність, а тому закономірно змінюються властивості елементів: зменшуються їхні неметалічні властивості й окислювальна здатність і посилюються металічні властивості.
Халькогени утворюють леткі сполуки з Гідрогеном із загальною формулою Н2Е. Це задушливі гази (крім води), при розчиненні яких у воді утворюються відповідні слабкі кислоти. У ряду кислот H2S → H2Se → Н2Те відбувається зростання сили кислот.
Елементи групи утворюють кислотні оксиди складу ЕO2 та ЕО3, яким відповідають гідроксиди – кислоти Н2ЕO3 та Н2ЕO4. У ряду кислот H2SO4 → H2SeO4 → Н2ТеO4 сила кислот спадає.
________________________________________________________________
1 За новою номенклатурою – 16 групи.
2 Халькогени (від гр. χαλκος – руда і γενος – рід) – “ті, що народжують руди”.
3 Дж. Н. Льюїс 1919 p., вивчаючи магнітні властивості розчинів кисню в рідкому азоті, виявив молекули чотирьохатомного Оксигену O4.