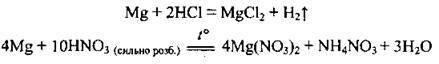Магній – Металічні елементи головної підгрупи II групи
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ
8. Металічні елементи та їхні сполуки. Метали
8.3. Металічні елементи головної підгрупи II групи1
8.3.2. Магній
Магній – 12-й елемент періодичної таблиці, заряд ядра – +12. Хімічний символ – Mg, відносна атомна маса – 24. Відомо три стабільні природні ізотопи Магнію: 24Mg (78,6 %), 25Mg (10,1 %), 26Mg (11,3 %). Утворює просту речовину магній. Виявляє валентність II і ступінь окиснення +2, утворює іон Mg2+.
Електронні формули:
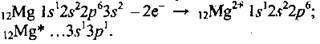
Поширеність у природі
Магній – 8-й за поширеністю елемент земної кори (1,87 % маси, тобто його кларк – майже 19 кг/т). Трапляється у вигляді мінералів магнезиту MgCO3, доломіту MgCO3 · СаСO3, карналітуMgCl2 · КСl · 6Н2O, каїніту КСl · MgSO4 · 3Н2O, бішофіту MgCl2 · 6Н2O. До складу основних порід також входять силікати: тальк 3MgO · 4SiO2 · Н2O, азбест СаО · 3MgO · 4SiO2 тощо. Багато його у морській воді – 0,12-0,13 % (саме йон Mg2+ надає їй гіркоти). Входить до складу хлорофілу (2,7 %).
Фізичні властивості магнію
Магній – пластичний сріблясто-білий метал. Його густина при 20 °С – 1,737 г/см3 (на третину менша за густину алюмінію, а міцність
Добування магнію
Магній добувають:
А) електролітичним розкладом карналіту або магній хлориду:
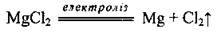
Б) відновленням з його оксиду за допомогою аморфного вуглецю за температури 2000 °С:
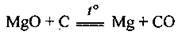
Хімічні властивості магнію
Метал дуже активний, на повітрі (подібно до алюмінію) вкривається оксидною плівкою, подальше окиснення можливе лише при нагріванні (> 300 °С). У хімічних реакціях виступає як сильний відновник. Магній реагує:
1) із простими речовинами:
– з киснем (горить яскравим полум’ям):
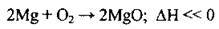
– з усіма неметалами (подібно до Кальцію):
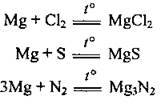
2) зі складними речовинами:
– з карбон(ІV) оксидом:
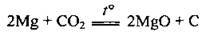
Отже, магній, який горить, не можна гасити вуглекислотним вогнегасником;
– з водою при нагріванні реагує дуже повільно через утворення малорозчинного гідроксиду:
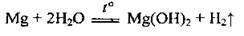
Але з водяною парою реагує легко:
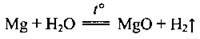
– з оксидами і галогенідами багатьох металічних елементів, легко відбираючи Оксиген і галогени:
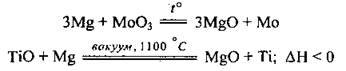
– з кислотами: