Анілін – АЗОТОВМІСНІ ОРГАНІЧНІ СПОЛУКИ
ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ
Частина III. ОРГАНІЧНА ХІМІЯ
Розділ 18. АЗОТОВМІСНІ ОРГАНІЧНІ СПОЛУКИ
§ 18.3. Анілін
Найпростішим представником ароматичних амінів є анілін C6H5NH2. Його можна розглядати як похідне бензолу, в молекулі якого атом водню заміщений аміногрупою, або як похідне аміаку, в молекулі якого один атом водню заміщено радикалом фенілом. Структурна формула аніліну така:
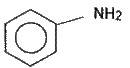
Анілін – безбарвна масляниста рідина із слабким характерним запахом. Він трохи важчий
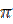 -Електрони бензольного ядра, вступаючи у взаємодію з неподіленою електронною парою азоту, притягують її у свою сферу і відтягують на себе. Як наслідок цього на атомі азоту зменшується електронна густина, слабкіше зв’язується протон і менше утворюється вільних гідроксильних іонів. Тому анілін виявляє дуже слабкі основні властивості (вони виражені слабше, ніж у амінів насиченого ряду і аміаку). Наприклад, розчин аніліну не забарвлює лакмус у синій колір,
-Електрони бензольного ядра, вступаючи у взаємодію з неподіленою електронною парою азоту, притягують її у свою сферу і відтягують на себе. Як наслідок цього на атомі азоту зменшується електронна густина, слабкіше зв’язується протон і менше утворюється вільних гідроксильних іонів. Тому анілін виявляє дуже слабкі основні властивості (вони виражені слабше, ніж у амінів насиченого ряду і аміаку). Наприклад, розчин аніліну не забарвлює лакмус у синій колір,C6H5NH2 + НСl −> (С6Н5NН3)Сl, або C6H5NH2 ∙ НСl.
Хлорид Солянокислий
Феніл амонію анілін
Солянокислий анілін добре розчинний у воді. Якщо до такого розчину додати достатню кількість розчину лугу, то анілін знову виділиться у вільному стані:
C6H5NH2 ∙НСl + NaOH -> C6H5NH2 + NaCl + Н2О.
Значний вплив на бензольне ядро має аміногрупа. Це виявляється на збільшенні рухливості водневих атомів порівняно з бензолом. Так, анілін легко взаємодіє з бромною водою за звичайних умов – без каталізатора і нагрівання:
C6H5NH2 + ЗВr2 -> C6Br3NH2 + ЗНВr.
З цієї самої причини анілін легко окиснюється. На повітрі анілін швидко буріє внаслідок окиснення. Легко взаємодіє з іншими окисниками, утворюючи речовини різного забарвлення. Так, при взаємодії аніліну з хлорним вапном з’являється характерне фіолетове, забарвлення. Це одна з найбільш чутливих якісних реакцій на анілін. При взаємодії аніліну з хромовою сумішшю (суміш концентрованої сульфатної кислоти і дихромату калію К2Сr2O7) утворюється чорний осад, який називають чорним аніліном. Останній застосовують як міцний барвник (для фарбування тканин і хутра у чорний колір). Звичайно тканину спочатку просочують розчином окисника. Чорний анілін, що утворюється, відкладається у порах волокна. Він не розчинний у воді і стійкий до дії мила і світла.
Добування. Анілін та інші первинні ароматичні аміни добуто за допомогою реакції, яку відкрив ще у 1842 р. знаменитий російський хімік М. М. Зінін. Реакція Зініна – це метод добування ароматичних амінів (у тому числі й аніліну) відновленням нітросполук. Слід підкреслити, що відновлення нітросполук є загальним, але не єдиним способом добування амінів.
М. М. Зінін використав як відновник сульфід амонію:
C6H5NO2 + 3(NH4)2S -> C6H5NH2 + 3S + 6NH3 + 2Н2О.
Однак потім як відновник почали застосовувати водень. Останнім часом основним промисловим способом добування аніліну є відновлення нітробензолу чавунними стружками за наявності невеликої кількості хлоридної кислоти (її звичайно заміняють хлоридом амонію). Цей процес можна представити рівнянням
4C6H5NO + 9Fe + 4Н2О -> 4C6H5NH2 + 3Fe3O4.
Останнім часом і цей спосіб поступово витісняється більш перспективним контактним способом – пропусканням суміші парів нітробензолу і водню над каталізатором при 800 °С:
C6H5NO2 + ЗН2 −> C6H5NH2 + 2Н2O.
Реакцією Зініна анілін добувають у великих кількостях. Таким же способом добувають і інші ароматичні аміни, наприклад толуїдини з нітротолуолів. Анілін і толуїдини є вихідними продуктами для добування анілінових барвників, лікарських речовин і багатьох інших цінних сполук.
Відкрите М. М. Зініним перетворення ароматичних нітросполук на аміни дало початок новій епосі у хімічній промисловості і стало поштовхом для бурхливого розвитку промисловості органічного синтезу, особливо анілінофарбової і фармацевтичної промисловості. “Якби Зінін не зробив нічого більше, крім перетворення нітробензолу на анілін, то й тоді його ім’я залишилось би записаним золотими буквами в історії хімії”, – так закінчив свою промову, присвячену пам’яті М. М. Зініна, у 1880 р. президент Німецького хімічного товариства, засновник німецької анілінофарбової промисловості А. В. Гофман.