Проміжне оцінювання навчальних досягнень з теми “Вуглеводні”
Тема 3
НАЙВАЖЛИВІШІ ОРГАНІЧНІ СПОЛУКИ
Урок 43
Тема уроку. Проміжне оцінювання навчальних досягнень з теми “Вуглеводні”
Цілі уроку: узагальнити та скоригувати знання учнів з теми “Вуглеводні”; визначити рівень навчальних досягнень учнів з теми, розуміння основних понять, уміння використовувати їх на практиці.
Тип уроку: контролю й коригування знань, умінь і навичок.
Форми роботи: письмова самостійна робота за варіантами.
Обладнання: картки-завдання.
ХІД УРОКУ
I. Організація класу
II. Письмова контрольна
Учитель розподіляє учнів за варіантами й нагадує їм зміст завдань, час виконання, ключові моменти оформлення відповідей і систему оцінювання:
– завдання 1-6 – тестові, кожне завдання оцінюється в 0,5 бала, загалом перші шість завдань – 3 бали;
– завдання 7-9 оцінюються по 2 бали кожне, загалом за дев’ять правильно виконаних завдань – 9 балів;
– завдання 10 пропонується виконувати учням, які претендують на оцінку 12 балів, оцінюється в 3 бали.
Отже, максимальна оцінка за правильно виконану роботу становить 12 балів.
Час на виконання роботи – 40 хв.
III. Домашнє завдання
Повторити
Варіант І
1. Загальна формула етиленових вуглеводнів – …
2. Гібридизація – це явище змішування. з утворенням однакових…
3. Назвіть тип ізомерії, характерний для алкінів:
А) структурна;
Б) положення кратного зв’язку;
В) просторова;
Г) міжкласова.
4. Установіть відповідність.
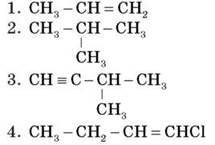
A. 2-метилпропан
Б. Пропен
B. 1-хлор-1-бутен
Г. 3-метил-1-бутин
5. Реакція описується рівнянням: 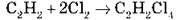
Укажіть, який об’єм хлору приєднається до 5 л ацетилену:
А) 5 л;
Б) 10 л;
В) 2,5 л;
Г) 22,4 л.
6. Метан застосовують:
А) як паливо;
Б) як ліки;
В) для зварювання металів;
Г) як сировину хімічного синтезу.
7. Напишіть два ізомери та два найближчі гомологи до речовини:
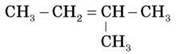
8. Напишіть рівняння реакцій, необхідних для здійснення перетворень:
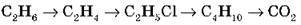
9. Визначте молекулярну формулу вуглеводню, якщо масова частка Гідрогену в ньому становить 17,2 %, а відносна густина за азотом – 2,07.
10. Обчисліть об’єм етану, який можна одержати в результаті взаємодії 10 л етилену й 5 л водню (н. у.).
Варіант ІІ
1. Загальна формула гомологічного ряду алканів – …
2. Гомологічний ряд – це послідовність речовин, що подібні за… та відрізняються…
3. Назвіть тип ізомерії, характерний для алкенів:
А) структурна;
Б) положення кратного зв’язку;
В) просторова;
Г) міжкласова.
4. Установіть відповідність.
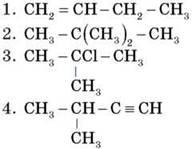
A. 3-метил-1-бутин
Б. 2-хлор-2-метилпропан
B. 1-бутен
Г. 2,2-диметилпропан
5. Реакція описується рівнянням: С2Н4 + Н2 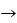 C2H6
C2H6
Укажіть об’єм водню, необхідний для повного гідрування 7 л етилену за рівнянням:
А) 7 л;
Б) 6 л;
В) 14 л;
Г) 3,5 л.
6. Ацетилен застосовують:
А) як паливо;
Б) як ліки;
В) для зварювання металів;
Г) як сировину хімічного синтезу.
7. Напишіть два ізомери й два найближчі гомологи до речовини:
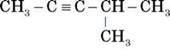
8. Напишіть рівняння реакцій, необхідних для здійснення перетворень:
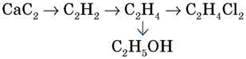
9. Визначте молекулярну формулу вуглеводню, якщо масова частка Карбону в ньому становить 90 %, а відносна густина за гелієм дорівнює 30.
10. Обчисліть об’єм повітря, що знадобиться для спалювання суміші, яка складається з 5 л етилену й 7 л ацетилену (н. у.).
Варіант ІІІ
1. Загальна формула ацетиленових вуглеводнів – …
2. Ізомерія – це явище існування речовин з однаковими. і різним…
3. Назвіть тип ізомерії, характерний для алканів:
А) структурний;
Б) положення кратного зв’язку;
В) просторовий;
Г) міжкласовий.
4. Установіть відповідність:
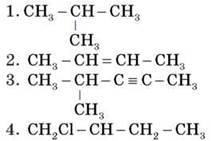
A. 1-хлор-2-метилбутан
Б. 1-бутен
B. 2-метилпропан
Г. 4-метил-2-бутин
5. Реакція описується рівнянням: CH4 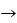 C + 2H2
C + 2H2
Укажіть об’єм водню, що виділиться в результаті термічного розкладу метану:
А) 22,4 л;
В) 12 л;
Б) 6 л;
Г) 24 л.
6. Етилен застосовують:
А) у медицині;
Б) для зварювання металів;
В) як розчинник;
Г) як сировину хімічного синтезу.
7. Напишіть два ізомери й два найближчі гомологи до речовини:
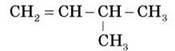
8. Напишіть рівняння реакцій, необхідних для здійснення перетворень:
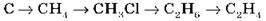
9. Визначте молекулярну формулу вуглеводню, якщо масова частка Карбону в ньому становить 85,68 %, а відносна густина за вуглекислим газом дорівнює 1,27.
10. Обчисліть об’єм етилену, який можна одержати з 25 л ацетилену й 15 л водню (н. у.).