Розмаїтість речовин. Метали й неметали
Тема 1
ПОЧАТКОВІ ХІМІЧНІ ПОНЯТТЯ
Урок 9
Тема. Розмаїтість речовин. Метали й неметали
Цілі уроку: ввести поняття про різноманіття речовин; дати початкову класифікацію елементів на метали й неметали, їх поширення в природі; навчити розрізняти металічні й неметалічні елементи за їх положенням у періодичній системі; показати істотну відмінність фізичних і хімічних властивостей металів і неметалів.
Тип уроку: комбінований.
Форми роботи: бесіда, евристична бесіда, розповідь, демонстрація, самостійна робота.
Обладнання:
ХІД УРОКУ
I. Організація класу
II. Перевірка домашнього завдання, актуалізація опорних знань
Чотири учні описують на дошці будову атома.
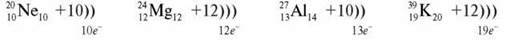
1) Скільки елементів знаходиться в періодичній системі? (Сто десять)
2) Які елементи зустрічаються переважно в космосі? (Н, Не)
3) Які елементи першими стали відомими людям? (Au, Ag, Cu, Fe, Sn, Pb, Hg)
4) Хто може пояснити, чому саме ці елементи першими навчилася використовувати
5) Речовин на Землі набагато більше, ніж елементів. Чому? (Елементи утворюють сполуки – молекули)
6) З яких частинок може складатися речовина? (Атоми, молекули, іони)
Розповідь учителя
Розгляньмо кристалічні гратки.
Алмаз: у вузлах граток атоми Карбону С.
Вуглекислий газ: у вузлах граток молекули карбон(ІІ) оксиду CO2. Натрій хлорид: у вузлах граток іони – катіони Натрію Na + та аніони Хлору Cl-.
Отже, речовини можуть складатися як з окремих атомів, так і з молекул, або заряджених частинок – іонів.
Тому

ІІІ. Вивчення нового матеріалу
Будова речовини залежить від природи хімічних елементів, що його утворюють.
Перша класифікація хімічних елементів за властивостями передбачає їх поділ на метали й неметали.
Демонстрація 9. Розгляд зразків металів і неметалів.
Розгляньмо колекцію “Метали”.
1. Які загальні властивості мають метали?
– Металевий блиск;
– сірі (крім міді);
– тверді;
– проводять електричний струм.
2. Розгляньмо зразки неметалів: сірка, графіт, ампула з кристалами I2. Додамо наші знання про N2 і O2.
– Крихкі;
– тверді або газоподібні;
– різні властивості.
Запишемо приклади:
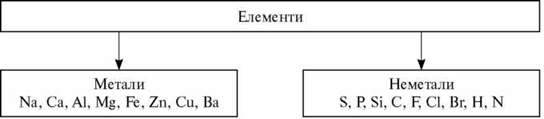
Розгляньмо діаграму поширення елементів (урок 6).
1) Яких елементів у космосі більше – металів чи неметалів? (Неметалів – H, He )
2) Частка яких елементів більша в земній корі – металів чи неметалів? (Неметалів: ?(O) = 47 %; ?(Si) = 27,6 %)
3) А які елементи містяться в повітрі? (Неметали Нітроген, Оксиген у складі речовин N2, O2)
А тепер подивімося в періодичну систему. Умовна діагональ від Бору до Астату поділяє періодичну систему на дві частини: у нижній частині таблиці ліворуч від діагоналі знаходяться елементи-метали, а у верхній лівій частині знаходяться елементи-неметали (крім елементів побічних груп).
Відомі також елементи, що в сполуках виявляють властивості як металів, так і неметалів. Вони називаються перехідними елементами. До них належать, наприклад, Fe, Ge та інші.
Окрема група елементів – це елементи головної підгрупи VIII групи: He, Ne, Ar, Kr, Xe, Rn. їх називають інертними, або благородними, елементами, оскільки вони не виявляють ні властивостей металів, ні властивостей неметалів.
3. Робота в парах
Запропонуйте по п’ять прикладів елементів металів і неметалів з періодичної системи.
Обміняйтеся знаннями і перевірте з допомогою періодичної системи, чи правильно виконане завдання в сусідніх пар.
IV. Підбиття підсумків
Оцінимо роботу пар.
Підіб’ємо підсумки уроку, уточнимо:
– На які дві групи поділяються хімічні елементи?
– Як розрізнити за положенням у періодичній системі металеві й неметалічні елементи?
– Чи можна за властивостями – хімічними чи фізичними – розрізнити, метал чи неметал?
V. Домашнє завдання
Прочитати параграф, відповісти на запитання.
Творче завдання. Скласти таблицю відмінностей фізичних властивостей металів і неметалів на підставі матеріалу підручника і своїх спостережень.