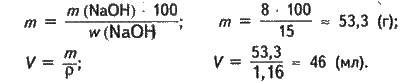Розв’язування типових задач – КИСНЕВМІСНІ ОРГАНІЧНІ СПОЛУКИ
ПОСІБНИК З ХІМІЇ ДЛЯ ВСТУПНИКІВ ДО ВИЩИХ НАВЧАЛЬНИХ ЗАКЛАДІВ
Частина III. ОРГАНІЧНА ХІМІЯ
Розділ 17. КИСНЕВМІСНІ ОРГАНІЧНІ СПОЛУКИ
§ 17.19. Розв’язування типових задач
Задача 1. Етанол об’ємом 30 мл (густина 0,79 г/мл) нагріли з надлишком броміду натрію і сульфатної кислоти. З реакційної суміші виділили брометан масою 42,3 г. Обчисліть масову частку виходу брометану.
Розв’язання. При нагріванні суміші етанолу з бромідом калію та сульфатною кислотою відбуваються реакції:
2KBr + H2SO4 ⇆ 2HBr + K2SO4; (а)
С2Н5ОН + НВr ⇆ С2Н5Вr + Н2O.
Брометан
Обчислюємо масу і кількість речовини етанолу, взятого для реакції:
M(С2Н5ОН) = V(С2Н5ОН) ∙ р(С2Н5OН);
M(С2Н5OН) = 30 ∙ 0,79 ≈ 23,7 (г);
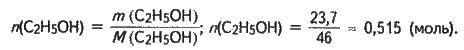
Із рівняння реакції (б) випливає:
N(С2Н5Вr) = n(С2Н5ОН); n(С2Н5Вr) = 0,515 (моль).
Розраховуємо масу брометану, який міг би утворитися при 100 %-му виході:
M(С2Н5Вr) = n(С2Н5Вr) ∙ M(С2Н5Вr);
M(С2Н5Вr) = 0,515 ∙ 109 ≈56,1 (г).
Обчислюємо масову частку виходу брометану:
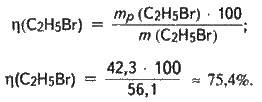
Задача 2. Як, виходячи з етану, добути етилацетат. Напишіть рівняння відповідних реакцій.
Розв’язання. Бромуванням етану спочатку одержуємо брометан:
С2Н6
Проводячи гідроліз брометану в присутності лугу, одержуємо етанол:
С2Н5Вr + Н2О -> С2Н5ОН + НВr (луг потрібний для зміщення рівноваги в бік спирту).
Зі спирту можна добути альдегід двома шляхами:
А) дегідруванням спирту:
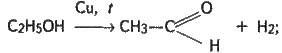
Б) окисненням спирту:
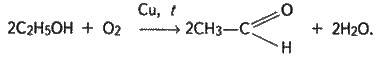
Окиснюючи альдегід (будь-яким окисником), можна одержати оцтову кислоту:
5СН3СНО + 2КМnO4 + 3H2SO4 −>5СН3СООН + 2MnSO4 + K2SO4 + ЗН2О.
Естер (складний ефір) – етилацетат – одержуємо з етанолу і оцтової кислоти за реакцією етерифікації в присутності каталізатора – концентрованої сульфатної кислоти:
С2Н5ОН + СН3СООН ⇆ С2Н5ОСОСН3 + Н2O.
Задача 3. Масова частка крохмалю у картоплі становить 20 %. Розрахуйте масу глюкози, яку можна добути з картоплі масою 405 кг. Вихід продукту дорівнює 70 %.
Розв’язання. Складаємо рівняння реакції гідролізу крохмалю, в результаті якої утворюється глюкоза:
(С6Н10О5)x: + хН2O -> xС6Н12О6.
Крохмаль Глюкоза
Розраховуємо масу крохмалю в картоплі:
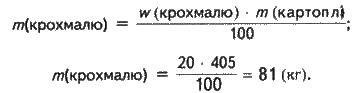
Визначаємо кількість речовини крохмалю:
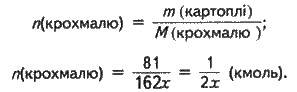
Із рівняння реакції гідролізу крохмалю випливає:
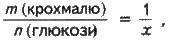
Звідки дістаємо:
N(глюкози) = х – n (крохмалю); n(глюкози) = 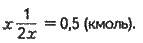
Обчислюємо масу глюкози, яку можна добути при кількісному виході:
M(глюкози) = n(глюкози) ∙ М(глюкози);
M(глюкози) = 0,5 ∙180 = 90 (кг).
Враховуючи масову частку виходу продукту, обчислюємо масу фактично добутої глюкози:
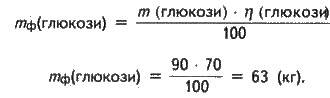
Задача 4. Одноосновна карбонова кислота має такий склад: вуглець (масова частка 40,0%), кисень (53,3%), водень (6,7%). Визначте формулу цієї кислоти. Обчисліть об’єм розчину гідроксиду натрію (масова частка NaOH 15%, густина 1,16 г/мл), який потрібний для нейтралізації зразка цієї кислоти масою 12 г.
Розв’язання. Формулу одноосновної карбонової кислоти можна представити у вигляді СxHyСНООН або Сx+1Нy+1О2. Обираємо для розрахунків зразок кислоти масою 100 г. Обчислюємо маси і кількості речовин С, Н і О у цьому зразку:
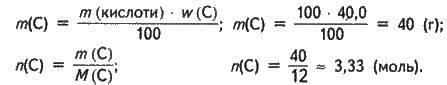
Аналогічно одержуємо, що n(Н) = 6,7 моль, n(О) = 3,33 моль.
Коефіцієнти у формулі кислоти дорівнюватимуть:
(х + 1) : (у + 1) : 2 = n(С) : n(Н) : n(O);
(х+ 1) : (у + 1) : 2 = 3,33 : 6,7 : 33,3 = 2:4:2.
Звідси випливає, що х + 1 = 2; х = 1; у + 1 = 4; у = З,
Тобто формула кислоти СН3СООН. Це – оцтова кислота.
Записуємо рівняння реакції нейтралізації цієї кислоти гідроксидом натрію:
СН3СООН + NaOH -> СН3СООNa + Н2О.
З умови задачі випливає, що для нейтралізації взято зразок кислоти масою 12 г, тобто m(СН3СООН) =12 г.
Визначаємо кількість речовини кислоти:
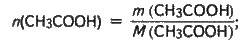
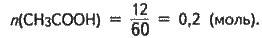
Із рівняння реакції виходить:
N(NaOH) = n(СН3СООН); n(NaOH) = 0,2 моль.
Обчислюємо масу гідроксиду натрію, яка реагує з кислотою:
M(NaOH) = n(NaOH) ∙ M(NaOH); m(NaOH) = 0,2 – 40 = 8 (г).
Розраховуємо масу і об’єм розчину NaOH, потрібного для нейтралізації кислоти: