Фенол, його склад, будова. Фізичні властивості фенолу. Хімічні властивості: взаємодія з натрієм, розчином лугу, бромною водою, ферум(ІІІ) хлоридом. Взаємний вплив атомів у молекулі фенолу
II Семестр
Тема 4. ОКСИГЕНОВМІСНІ ОРГАНІЧНІ СПОЛУКИ
Урок 33
Тема уроку. Фенол, його склад, будова. Фізичні властивості фенолу. Хімічні властивості: взаємодія з натрієм, розчином лугу, бромною водою, ферум(ІІІ) хлоридом. Взаємний вплив атомів у молекулі фенолу
Цілі уроку: розширити уявлення учнів про оксигеновмісні органічні сполуки на прикладі фенолів; ознайомити з молекулярними, електронними й структурними формулами фенолу та його гомологів, фізичними властивостями, зумовленими наявністю бензольного кільця й функціональної
Тип уроку: вивчення нового матеріалу.
Форми роботи: фронтальна робота, навчальна лекція, робота з підручником (таблицею), демонстраційний експеримент.
Демонстрація 4. Розчинність фенолу у воді за кімнатної температури й нагрівання.
Демонстрація 5. Одержання натрій феноляту.
Демонстрація 6. Витиснення фенолу з натрій феноляту дією
Демонстрація 7. Взаємодія фенолу з ферум(ІІІ) хлоридом.
Обладнання: медіа-фрагмент про будову фенолу.
ХІД УРОКУ
I. Організація класу
II. Актуалізація опорних знань.
Мотивація навчальної діяльності
Фронтальна робота
1) Назвіть види гібридизації атомів Карбону.
2) Опишіть механізм утворення хімічного зв’язку в бензольному кільці.
3) Як впливає на властивості бензену наявність сполученого п-зв’язку?
4) Чи можлива наявність функціональних груп у бензольному кільці? Як впливатимуть ці групи на властивості сполук, що утворилися?
III. Вивчення нового матеріалу
ФЕНОЛИ
1. Феноли
Феноли – це гідроксисполуки, у молекулах яких є одна або кілька ОН-груп, сполучених безпосередньо з бензольним кільцем.
У фенолах під впливом п-електронної системи бензольного кільця атом Оксигену перебуває в стані sp2-гібридизації. При цьому одна з неподілених електронних пар знаходиться на негібридній р-орбіталі й може брати участь у сполученні з ароматичною п-системою.
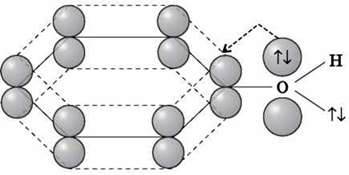
Розглядаємо схему або переглядаємо медіа-фрагмент про будову молекули фенолу та взаємний вплив бензольного кільця й гідроксильної групи.
2. Класифікація фенолів
За числом гідроксильних груп, приєднаних до кільця, феноли поділяються на одно-, дво – й багатоатомні.
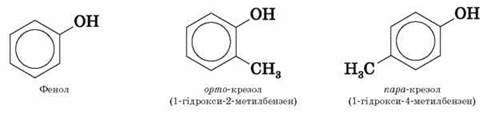
Серед багатоатомних фенолів найпоширеніші двохатомні:
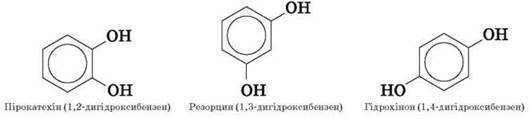
Фенолам властива структурна ізомерія, зумовлена взаємним положенням замісників у бензольному кільці.
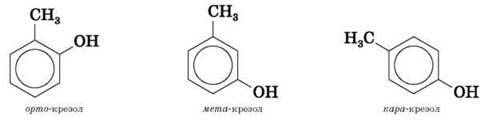
Завдання. Побудуйте ізомери складу C8H9 – OH. Назвіть їх.
3. Фізичні властивості фенолу
Властивості фенолів визначаються будовою гідроксильної групи, характером її хімічних зв’язків, будовою вуглеводневих радикалів та їхнім взаємним впливом.
Демонстрація 4. Розчинність фенолу у воді за кімнатної температури й нагрівання
Водний розчин фенолу називається карболовою кислотою.
4. Одержання фенолів
Фенол у промисловості одержують:
1) окисненням ізопропілбензену (кумолу) у гідропероксид з наступним розкладанням її сульфатною кислотою:
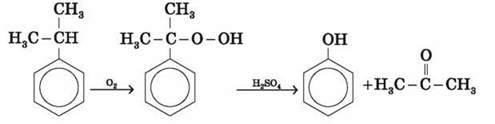
2) з бензену за способом Рашига:
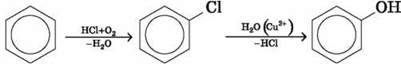
5. Хімічні властивості фенолу
¦ Порівняйте розподіл електронної густини й особливості хімічного зв’язку в молекулах метанолу й фенолу.
Феноли є більш сильними кислотами, ніж спирти й вода, оскільки за рахунок участі неподіленої електронної пари кисню в поєднанні з п-електронною системою бензольного кільця полярність зв’язку O – H збільшується.
Демонстрація 5. Одержання натрій феноляту
Феноли реагують з гідроксидами лужних і лужноземельних металів, утворюючи солі – феноляти:
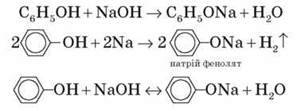
Демонстрація 7. Взаємодія фенолу з ферум(ІІІ) хлоридом
Для виявлення фенолів використовується якісна реакція з ферум(ІІІ) хлоридом. Одноатомні феноли дають стійке синьо-фіолетове забарвлення, що пов’язано з утворенням комплексних сполук Феруму.
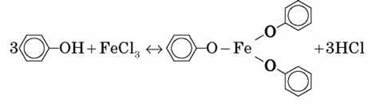
Демонстрація 6. Витіснення фенолу з натрій феноляту дією вуглекислого газу
Феноли – дуже слабкі кислоти, тому феноляти легко гідролізуються й руйнуються не лише сильними, але й дуже слабкими кислотами:
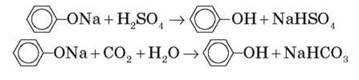
*Феноли не утворюють естерів у реакціях з кислотами. Для цього використовуються більш реакційноздатні похідні кислот (ангідриди, хлорангідриди).
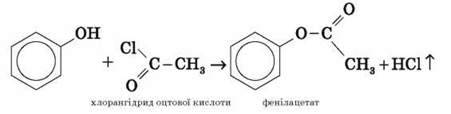
Для фенолів не характерні реакції за зв’язком C – O, оскільки атом Оксигену міцно зв’язаний з атомом Карбону бензольного кільця за рахунок участі своєї неподіленої електронної пари в системі сполучення.
Реакції фенолу за бензольним кільцем
Взаємний вплив атомів у молекулі фенолу виявляється не лише в особливостях поводження гідроксигрупи, але й у більшій реакційній здатності бензольного ядра. Гідроксильна група підвищує електронну густину в бензольному кільці, особливо в орто – й пара – положеннях:
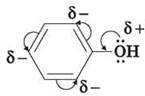
Тому фенол значно активніше за бензен вступає в реакції електрофільного заміщення в ароматичному кільці.
Нітрування
Під дією нітратної кислоти HNO3 фенол легко перетворюється на суміш орто – і пара-нітрофенолів:
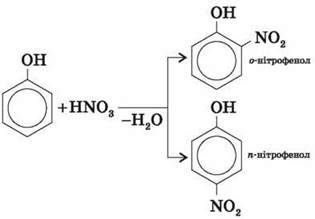
У разі використання концентрованої HNO3 утворюється 2,4,6-тринітрофенол (пікринова кислота):
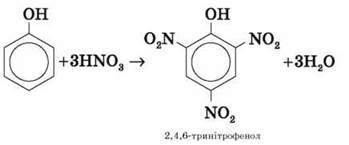
Галогенування
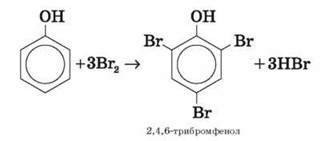
Фенол легко, за кімнатної температури, взаємодіє з бромною водою з утворенням білого осаду 2,4,6-трибромфенолу (якісна реакція на фенол):
IV. Застосування одержаних знань
1. Фронтальна бесіда
¦ Чи можна стверджувати, що феноли належать до органічних кислот?
¦ Виходячи з фізичних і хімічних властивостей фенолу, запропонуйте способи його використання.
2. Застосування фенолів
Фенол застосовується у виробництві феноло-формальдегідних смол, у фармацевтичній промисловості та як антисептик (карболова кислота).
Гідрохінон (1,4-діоксибензен) – проявник у фотографії.
3. розв’язування задач
1) Обчисліть масу нітратної кислоти, потрібної для нітрування фенолу масою 18,8 г до 2,4,6-тринітрофенолу.
2) Натрій фенолят кількістю речовини 0,3 моль повністю прореагував з розчином хлоридної кислоти масою 120 г з масовою часткою речовини 40 %. Яка маса фенолу утворилася?
3) До суміші фенолу з бензеном масою 50 г долили бромну воду в надлишку. Випав білий осад масою 99,3 г. Обчисліть масову частку речовин у вихідній суміші.
V. Підбиття підсумків уроку
Учитель узагальнює відповіді, оцінює роботу учнів на уроці.
VI. Домашнє завдання
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
Творче завдання: підготувати повідомлення про використання фенолів і охорону навколишнього середовища від забруднення фенолами.
