Загальна характеристика – Урок 2 – Металічні елементи головної підгрупи II групи
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ
8. Металічні елементи та їхні сполуки. Метали
8.3. Металічні елементи головної підгрупи II групи1
8.3.1. Загальна характеристика
Лужноземельні металічні елементи – це s-елементи, які розміщуються у головній підгрупі II групи періодичної системи, а саме: Кальцій (Са), Стронцій (Sr), Барій (Ва), Радій (Ra). Інші елементи головної підгрупи – це Берилій (Be) та Магній (Mg).
Електронна формула – ns2, у збудженому стані – ns1np1. Зі збільшенням
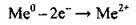
Хімічна активність елементів НА групи зростає зі збільшенням радіуса атома (від Берилію до Радію), і, відповідно, посилюються металічні властивості.
Прості
Усі лужноземельні метали мають сріблясто-білий колір, вони легкі, м’які, легкоплавкі, розрізаються ножем, мають хорошу електропровідність. На повітрі вкриваються шаром, який поряд з оксидами МеО містить пероксиди МеО2 і нітриди Me3N2. Через легкість окиснення на повітрі лужноземельні метали зберігають під шаром гасу.
Берилій утворює оксид і гідроксид, які мають амфотерні властивості. Усі інші елементи утворюють оксиди МеО та гідроксиди Ме(ОН)2, які виявляють основні властивості, що посилюються зі збільшенням порядкового номера елемента. Усі основи, крім Mg(OH)2 та Ве(ОН)2,- луги. Магній гідроксид розчиняється лише у гарячій воді; одержаний гідроксид при нагріванні взаємодіє з кислотними оксидами.
Леткі сполуки лужноземельних металічних елементів забарвлюють безбарвне полум’я в характерні кольори; сполуки Кальцію – у цегляно-червоний колір, Стронцію і Радію – у кармінно-червоний, Барію – у жовто-зелений.
___________________________________________________________
1 За новою номенклатурою – II групи.