Естери – Естери. Жири – Оксигеновмісні органічні сполуки
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ III. ОРГАНІЧНА ХІМІЯ
12. Оксигеновмісні органічні сполуки
12.5. Естери. Жири
12.5.1. Естери
Естери – це органічні сполуки, що утворюються внаслідок взаємодії карбонових кислот1 зі спиртами з відщепленням молекули води. Загальна формула:
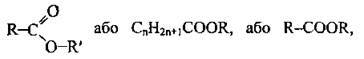
Де R – алкільний замісник або атом Гідрогену;
R’ – вуглеводневий залишок (аліфатичний, ароматичний).
Отже, у складі естерів можна виділити функціональну групу: 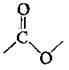
Номенклатура
Назви естерів за міжнародною номенклатурою утворюють від назви вуглеводневого замісника, що є у спирті, назви кислотного залишку і суфікса – оат:
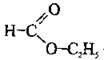 – етилметаноат (тривіальна назва – етилформіат)
– етилметаноат (тривіальна назва – етилформіат)
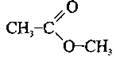 – метилетаноат (метилацетат, метиловий естер оцтової кислоти)
– метилетаноат (метилацетат, метиловий естер оцтової кислоти)
Ізомерія
Структурна:
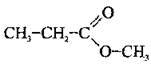 – метилпропаноат (метилпропіонат)
– метилпропаноат (метилпропіонат)
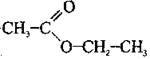 – етилетаноат (етилацетат)
– етилетаноат (етилацетат)
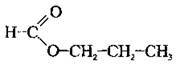 – пропілметаноат (пропілформіат)
– пропілметаноат (пропілформіат)
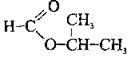 – ізопропілметаноат
– ізопропілметаноат
Міжкласова:
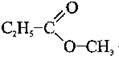 – метилпропаноат
– метилпропаноат
СН3-СН2-СН2-СООН – масляна кислота
Фізичні властивості
Естери – це переважно леткі безбарвні рідини з приємним фруктовим запахом, малорозчинні у воді. Унаслідок відсутності водневих зв’язків естери киплять за значно нижчих температур порівняно з кислотами і спиртами. Вищі естери – воскоподібні речовини, нерозчинні у воді, добре розчиняються в органічних розчинниках – бензині, хлороформі, етері.
Поширення в природі
Нижчі естери значною мірою визначають аромат квітів, плодів рослин. Деякі рослини, наприклад ясенець (рослина род. Рутових, старозавітна неопалима купина), виділяють таку кількість цих речовин, що навколо них утворюється естерова хмарка з ароматом, який нагадує лимонний.
Вищі естери становлять основу природних воскоподібних речовин. Розрізняють:
– бджолиний – виробляється спеціальними залозами медоносних бджіл, з якого вони будують сота;
– вовняний (ланолін) – виділяється залозами шкіри тварин, оберігає вовну і шкіру тварин від вологи, висихання і забруднення;
– спермацет – вміст “спермацетового” мішка у голові кашалотів, на який припадає до 90 % маси голови, найімовірніше бере участь в ехолокації, а також має низку інших функцій (зокрема пірнання);
– рослинні воски вкривають тонким шаром листя, стебла, плоди, оберігаючи їх від висихання, шкідників.
Хімічні властивості естерів
Гідроліз. Утворюється спирт і карбонова кислота чи її сіль – мило. Тому цю реакцію називають також реакцією омилення2:
А) кислотний (оборотний):
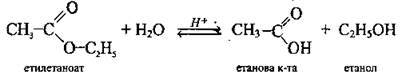
Б) лужний (необоротний):
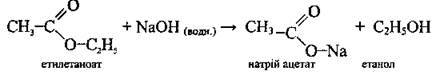
Добування естерів
1. Основний метод добування естерів – реакція етерифікації:
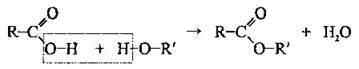
За допомогою мічених атомів (180) було доведено, що молекула води утворюється за рахунок саме гідроксильної групи кислоти й атома Гідрогену гідроксильної групи спирту.
2. Взаємодія ангідридів (або галогеноангіридів) кислот зі спиртами:
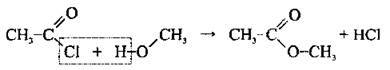
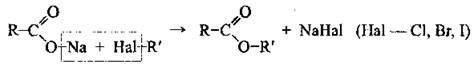
3. Взаємодія солей карбонових кислот з алкілгалогенідами:
Застосування естерів
Естери широко використовують у харчовій, парфумерній, фармацевтичній, хімічній промисловості для виготовлення фруктових есенцій (метилбутаноат має запах яблук, етилбутаноат – бананів, етилбензоат – м’яти), парфумів, лікарських препаратів, пластмас. Естери – добрі розчинники органічних речовин, зокрема лаків.
________________________________________________________________
1 Естери можуть утворювати і мінеральні кислоти, наприклад нітратна кислота, реагуючи з гліцеролом і целюлозою, утворює відповідно естери нітрогліцерол і нітроцелюлозу.
2 Число омилення – маса калій гідроксиду (у мг), яка необхідна для омилення 1 г естеру.