Тести – Урок 8
ХІМІЯ – Комплексна підготовка до зовнішнього незалежного оцінювання
РОЗДІЛ II. НЕОРГАНІЧНА ХІМІЯ
9. Неметалічні елементи та їхні сполуки. Неметали
Тести
9.1 Найдешевшим способом добування водню є конверсія (перетворення) метану з водяною парою. Який об’єм суміші газів утвориться при використанні 200 л метану?
А 0,2 м3
Б 0,8 м3
В 2 м3
Г 4 м3
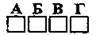
9.2 Проаналізуйте твердження і вкажіть правильні:
1. Водень можна зібрати витісненням води.
2. Водень збирають витісненням повітря в пробірці,
3. Водень збирають витісненням повітря в пробірці, розміщеній дном догори.
А правильне лише перше твердження
Б правильне лише друге твердження
В усі твердження є неправильними
Г правильне лише перше і третє твердження
9.3 Водень виявляє окислювальні властивості в реакції, що описують рівнянням

9.4 Укажіть речовину, за допомогою якої визначають чистоту водню
А кисень
Б озон
В хлор
Г азот
9.5 Об’єм водню, необхідний
А 89,6 л
Б 44,8 л
В 22,4 л
Г 112 л
9.6 Об’ємне співвідношення водню і кисню в гримучій суміші становить
А 2:3
Б 2:1
В 1:2
Г 1:1
9.7 Укажіть назву нукліда, у ядрі атома якого немає нейтронів
А Дейтерій
Б Оксиген
В Протій
Г Тритій
9.8 Установіть відповідність молярних мас продуктів реакції з такими реагентами
Реагенти: | Молярна маса продукту реакції: |
1 азот і водень | А 36,5 г/моль |
2 водень і хлор | Б 24 г/моль |
3 етен і водень | В 17 г/моль |
4 натрій і водень | Г 30 г/моль |
Д 28 г/моль |
9.9 Укажіть речовину, з якою взаємодіє водень за стандартних умов
А фтор
Б хлор
В бром
Г кисень
9.10 Укажіть найслабший окисник
А І2
Б Вr2
В Сl2
Г F2

9.11 Яку масу спиртового розчину йоду з масовою часткою йоду 5 % потрібно додати до 100 г спиртового розчину йоду з Масовою часткою речовини 12%, щоб одержати йодну настоянкуз масовою часткою йоду 10 %?
А 25 г
Б 30 г
В 40
Г 70 г

9.12 Укажіть назви речовин, які взаємодіють з хлоридною кислотою: 1) купрум(ІІ) оксид; 2) калій нітрат; 3) калій карбонат; 4) мідь; 5) купрум(ІІ) гідроксид; 6) калій сульфат
А 1, 2, 5
Б 1, 3, 5
В 1, 4, 5
Г 2, 4, 5

9.13 Установіть відповідність між назвами сполук та найважливішими галузями їхнього застосування
Назва: | Галузь: |
1 калій хлорид | А медицина |
2 натрій хлорид | Б дезінфекція води |
3 хлор | В добування органічних речовин |
4 гідрогенхлорид | Г сільське господарство |
Д металургія |

9.14 Укажіть формули речовин, які взаємодіють з хлором: 1) KF; 2) MgO; 3) Н2O; 4) КВr; 5) Ag; 6) Zn(NO3)2
А 3, 4, 5
Б 2, 4, 5
В 4, 5, 6
Г 1, 3, 4

9.15 Установіть відповідність між назвами природних сполук галогенів та їхніми формулами
Назва: | Формула: |
1 карналіт | A AlF3 · NaF |
2 галіт | Б CaF2 |
3 флюорит | В СаСl2 |
4 кріоліт | Г КСl · MgCl2 · 6Н2O |
Д NaCl |

9.16 Установіть послідовність зменшення радіуса атомів елементів, атоми яких мають електронну конфігурацію зовнішнього електронного шару
А…6s26p5
Б…2s22p5
В…4s24p5
Г…3s23р5
9.17 Укажіть електронну конфігурацію атома Хлору в третьому збудженому стані
A…3s23p5
Б…3s13р33d3
В…3s23p33d2
Г…3s23p23d3

9.18 Укажіть рівняння хімічної реакції, у якій Хлор виявляє властивості і Окисника, і відновника
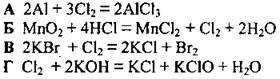

9.19 Укажіть галоген, який не виявляє в сполуках ступеня окиснення +7
А Флуор
Б Хлор
В Бром
Г Йод

9.20 Установіть послідовність зменшення хімічної активності галогенів
А бром
Б хлор
В йод
Г фтор

9.21 Укажіть речовини, з яких у лабораторних умовах можна добути сульфур(ІV) оксид:
1) калій і концентрована сульфатна кислота; 2) калій сульфат і нітратна кислота;
3) мідь і розбавлена сульфатна кислота; 4) калій сульфіт і хлоридна кислота;
5) мідь і концентрована сульфатна кислота; 6) сірка і кисень
А 3, 4, 5
Б 4, 5, 6
В 3, 5, 6
Г 2, 5, 6

9.22 Укажіть речовини, з яких у лабораторних умовах можна добути кисень: 1) калій сульфіт; 2) калій хлорат; 3) калій сульфід; 4) калій нітрат; 5) калій перманганат; 6) калій карбонат
А 1, 3, 4
Б 4, 5, 6
В 2, 4, 5
Г 3, 4, 5

9.23 Укажіть речовини, які можна використати для якісного виявлення сульфід-іона: 1) калій нітрат; 2) аргентум нітрат; 3) цинк сульфат; 4) калій гідроксид; 5) барій оксид; 6) плюмбум(ІІ) нітрат
А 1,3
Б 2,4
В 4,6
Г 2,6

9.24 Укажіть метали, які не взаємодіють з концентрованою сульфатною кислотою за стандартних умов: 1) алюміній; 2) мідь; 3) залізо; 4) хром; 5) цинк; 6) золото
А 2, 4, 5, 6
Б 2, 3, 5, 6
В 1, 3, 4, 6
Г 2, 3, 4, 5

9.25 Укажіть речовини, які взаємодіють з розбавленою сульфатною кислотою: 1) барій карбонат; 2) сульфідна кислота; 3) натрій хлорид; 4) силіцій(ІV) оксид; 5) алюміній; 6) барій нітрат
А 2, 4, 6
Б 1, 5, 6
В 2, 3, 6
Г 2, 4, 5

9.26 На основі наведених схем складіть рівняння реакцій і розташуйте їх у послідовності зменшення суми коефіцієнтів
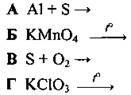

9.27 Укажіть формули речовин, ступінь окиснення неметалічного елемента в яких становить -1: 1) Сu2O; 2) FeS2; 3) Na2O2; 4) Р2O5; 5) Fe2O3; 6) Н2O2
А 1, 3, 4
Б 2, 3, 6
В 1, 2, 3
Г 3, 4, 5

9.28 Укажіть речовини, які взаємодіють із сульфур(VІ) оксидом: 1) HNO3; 2) NaOH; 3) Zn; 4) NO; 5) K2O; 6) H2O
А 2, 5, 6
Б 2, 3, 6
В 2, 4, 6
Г 4, 5, 6

9.29 Укажіть каталітичні реакції: 1) горіння дигідроген сульфіду; 2) окиснення сульфур(ІV) оксиду; 3) розкладання калій нітрату; 4) розкладання калій хлорату; 5) розкладання дигідрогенпероксиду; 6) окиснення цинк сульфіду
А 3, 4, 5
Б 4, 5, 6
В 1, 3, 5
Г 2, 4, 5

9.30 Укажіть протонне число елемента, який має на 8 електронів більше, ніж йон, утворений Оксигеном
А 17
Б 18
В 19
Г 20

9.31 Установіть відповідність між назвами природних сполук Сульфуру та їхніми формулами
Назва: | Формула: |
1 пірит | A CaSO4 · 2Н2O |
2 гіпс | Б Na2SO4 · 10Н2O |
3 глауберова сіль | В PbS |
4 свинцевий блиск | Г FeS2 |
Д FeS |

9.32 Установіть послідовність збільшення міцності хімічних зв’язків у молекулах сполук елементів головної підгрупи VI групи з Гідрогеном
A H2S
Б Н2O
В Н2Те
Г H2Se

9.33 Проаналізуйте твердження і вкажіть правильні:
1. Високу температуру кипіння води пояснюють ковалентною природою хімічних зв’язків у іі молекулах.
2. Високу температуру кипіння води пояснюють здатністю молекул води утворювати міжмолекулярні водневі зв’язки.
3. Високу температуру кипіння води пояснюють здатністю молекул води до дисоціації.
А правильні всі твердження
Б правильне лише перше твердження
В правильне лише друге твердження
Г усі твердження є неправильними

9.34 Проаналізуйте твердження і вкажіть правильні:
1. Продукт окиснення сірки киснем може виявляти лише окисні властивості.
2. Продукт окиснення сірки киснем може виявляти лише відновні властивості.
3. Продукт окиснення сірки киснем може виявляти і відновні, і окисні властивості.
А правильне лише друге твердження
Б правильне лише третє твердження
В правильне лише перше твердження
Г усі твердження є неправильними

9.35 Укажіть електронну конфігурацію зовнішнього електронного шару йонів, утворених елементами VIA групи
A ns2np3
Б ns2nр4
В ns2np5
Г ns2np6

9.36 На основі наведених схем складіть рівняння реакцій і розташуйте їх у послідовності зменшення суми коефіцієнтів
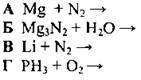
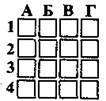
9.37 Укажіть суму коефіцієнтів хімічного рівняння термічного розкладання алюміній нітрату
А 18
Б 21
В 22
Г 24

9.38 Укажіть послідовність утворення сполук під час добування кальцій нітрату
А NO
Б NH3
В NO2
Г HNO3
9.39 Укажіть іон, валентність Нітрогену в якому становить IV, а ступінь окиснення – -3
А нітрат-іон
Б нітрит-іон
В іон амонію
Г іон гідроксонію

9.40 Укажіть формулу сполуки, валентність Нітрогену в якій становить IV, а ступінь окиснення – +5
A NH4OH
Б HNO3
В HNO2
Г N2O

9.41 Реакція азоту з воднем є
А гетерогенною, екзотермічною, необоротною, окисно-відновною
Б гомогенною, екзотермічною, оборотною, каталітичною, окисно-відновною
В гетерогенною, каталітичною, екзотермічною, необоротною, окисно-відновною
Г гомогенною, ендотермічною, необоротною, каталітичною

9.42 Укажіть дуже отруйні речовини: 1) NaNO3; 2) Р4; 3) NO; 4) (NH4)2CO3; 5) NO2
А 1, 4, 5
Б 2, 3, 5
В 2, 4, 5
Г 3, 4, 5

9.43 Укажіть речовини з молекулярними кристалічними гратками: 1) білий фосфор; 2) калій ортофосфат; 3) фосфор(V) оксид; 4) амоній нітрат; 5) нітроген(IV) оксид; 6) червоний фосфор
А 1, 2, 4
Б 2, 3, 5
В 1, 3, 5
Г 1, 3, 6

9.44 Установіть послідовність речовин відповідно до збільшення ступеня окиснення Фосфору
А фосфор(ІІІ) оксид
Б калій метафосфат
В калій фосфід
Г білий фосфор

9.45 Укажіть формули сполук, які відносіть до несолетвірних оксидів: 1) NO; 2) NH3; 3) NO2; 4) N2О; 5) N2О5
A 1,3
Б 1,4
В 2,5
Г 3,5

9.46 Яка дія сприятиме зміщенню хімічної рівноваги реакції, термохімічне рівняння якої: 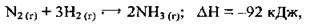 у бік утворення реагентів?
у бік утворення реагентів?
А зниження температури
Б зниження тиску
В підвищення концентрації азоту
Г зниження концентрації аміаку
9.47 Укажіть формулу оксиду, який, взаємодіючи з лугом, диспропорціонує, тобто і окислюється, і відновлюється
A N2О
Б NО2
В N2O5
Г NO

9.48 Укажіть схему хімічної реакції, у якій Нітроген є відновником


9.49 Укажіть масу купрум(ІІ) нітрату, при дисоціації якої утворюється 0,05 моль нітрат-іонів, якщо ступінь дисоціації становить 100 %
А 1,88 г
Б 3,4 г
В 4,7 г
Г 18,8 г

9.50 Напишіть рівняння реакції добування фосфору згідно зі схемою: 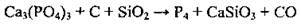 . Укажіть коефіцієнт перед відновником
. Укажіть коефіцієнт перед відновником
А 2
Б 8
В 10
Г 12

9.51 Укажіть речовину, яку зберігають у герметично закритій посудині
А калій нітрат
Б калій ортофосфат
В кальцій ортофосфат
Г фосфор(V) оксид

9.52 Установіть послідовність утворення сполук під час добування кальцій нітрату з азоту
A NO2
Б NO
В NH3
Г HNO3

9.53 Напишіть рівняння реакції добування фосфору згідно зі схемою: 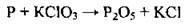 . Укажіть коефіцієнт перед окисником
. Укажіть коефіцієнт перед окисником
А 6
Б 5
В 4
Г 3

9.54 Укажіть речовини, які використовують при виробництві сірників: 1) фосфор(V) оксид; 2) бертолетова сіль; 3) калійна сіль; 4) сірка; 5) червоний фосфор; 6) білий фосфор
А 2, 4, 5
Б 1, 4, 5
В 2, 3, 4
Г 4, 5, 6

9.55 Установіть відповідність між назвами сполук та найважливішими галузями їхнього застосування
Назва: | Галузь: |
1 натрій нітрит | А виробництво барвників, кіно – і фотоплівки |
2 калій нітрат | Б як розпушувач тіста в харчовій галузі |
3 нітратна кислота | В виготовлення вибухових речовин |
4 амоній карбонат | Г як консервант у харчовій галузі |
Д будівництво |
9.56 Укажіть речовину, яка розкладається згідно зі схемою: 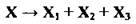
А амоній хлорид
Б амоній карбонат
В калій нітрит
Г амоній нітрат

9.57 Проаналізуйте твердження і вкажіть правильні:
1. Нашатирний спирт – це водний розчин амоній хлориду.
2. Нашатирний спирт – це водний розчин амоній карбонату.
3. Нашатирний спирт – це водний розчин аміаку.
А правильне лише перше твердження
Б правильне лише друге твердження
В правильне лише третє твердження
Г усі твердження є неправильними

9.58 Напишіть рівняння реакції взаємодії кальцію з нітратною концентрованою кислотою. Укажіть коефіцієнт перед окисником
А 10
Б 9
В 8
Г 6

9.59 Напишіть рівняння реакції взаємодії міді з розбавленою нітратною кислотою. Укажіть коефіцієнт перед відновником
А 3
Б 5
В 7
Г 8

9.60 Установіть відповідність між назвами сполук та найважливішими галузями їхнього застосування
Назва: | Галузь: |
1 ортофосфатна кислота | А виробництво товарів побутової хімії |
2 барій нітрат | Б виробництво сірників |
3 амоній дигідрогенортофосфат | В виробництво мінеральних добрив |
4 червоний фосфор | Г виробництво кормових добавок |
Д компонент піротехнічних сумішей |
9.61 Укажіть пару речовин, при взаємодії яких один з одержаних продуктів є сіллю амонію
А срібло і концентрована нітратна кислота
Б алюміній і дуже розбавлена нітратна кислота
В мідь і концентрована нітратна кислота
Г магній і концентрована нітратна кислота

9.62 Проаналізуйте твердження і вкажіть правильні:
1. Максимальна валентність Нітрогену – V, а найвищий ступінь окиснення – +5.
2. Максимальна валентність Нітрогену – IV, а найвищий ступінь окиснення – +5.
3. Максимальна валентність Нітрогену – V, а найвищий ступінь окиснення – +3.
А правильне лише друге твердження
Б правильне лише перше твердження
В правильне лише третє твердження
Г усі твердження є неправильними

9.63 Укажіть метал, з якого можна виготовити цистерну для транспортування концентрованої нітратної кислоти
А магній
Б цинк
В свинець
Г залізо

9.64 Хімічна реакція між калій гідроксидом і карбон(ІV) оксидом, кількості речовин яких співвідносяться як 1:1, є реакцією
А обміну
Б сполучення
В заміщення
Г розкладу

9.65 Укажіть електронну конфігурацію зовнішнього електронного шару атома Силіцію в збудженому стані
A 2s22p2
Б 3s23р2
В 3s23p4
Г 3s13р3

9.66 Установіть відповідність між алотропною видозміною Карбону та її будовою
Алотропна видозміна: | Будова: |
1 фулерен | А тетраедрична |
2 графіт | Б пірамідальна |
3 алмаз | В сферична |
4 карбін | Г лінійна |
Д шарувата |
9.67 Установіть послідовність зменшення радіусів атомів елементів, користуючись електронними конфігураціями зовнішнього електронного шару їхніх атомів
A 4s24р2
Б 5s25p2
В 6s26p2
Г 3s23p2
9.68 Установіть послідовність послаблення неметалічних властивостей, користуючись електронними конфігураціями зовнішнього електронного шару
А 5s25p2
Б 3s23p2
В 2s22p2
Г 4s24p2

9.69 Під час розчинення 32,4 г гідрогенкарбонату двовалентного елемента у хлоридній кислоті виділилось 8,96 л карбон(ІV) оксиду (н. у.). Укажіть протонне число невідомого елемента у складі солі
А 30
Б 20
В 12
Г 4
9.70 Установіть послідовність зменшення відносної густини за неоном газоподібних речовин
А чадний газ
Б вуглекислий газ
В метан
Г силан

9.71 Напишіть рівняння реакції відновлення ферум(ІІІ) оксиду чадним газом до заліза. Укажіть коефіцієнт біля відновника
А 3
Б 4
В 5
Г 6
9.72 Укажіть речовину, яку використовують як адсорбент
А сажа
Б графіт
В активоване вугілля
Г кокс
9.73 Установіть відповідність між назвами сполук та найважливішими галузями їхнього застосування
Назва: | Галузь: |
1 натрій карбонат | А виробництво вапна |
2 натрій гідрогенкарбонат | Б у металургії як відновник |
3 кальцій карбонат | В виробництво пластмас |
4 карбон(ІІ) оксид | Г виробництво скла |
Д як розпушувач тіста в харчовій галузі |

9.74 Укажіть речовини, які реагують з коксом: 1) купрум(І) оксид; 2) кисень; 3) калій гідроксид; 4) калій хлорид; 5) карбон(ІV) оксид; 6) купрум(ІІ) хлорид
А 1, 2, 3
Б 1, 2, 5
В 1, 3, 5
Г 2, 4, 5
9.75 Сіль А становить основу породи, яку використовують як оздоблювальний матеріал у будівництві. Під час термічного розкладання солі А утворюється газ Б, який бере участь у фотосинтезі. Укажіть хімічні формули речовин А і Б
А Са(НСO3)2, СO2
Б СаСO3, СO2
В СаО, СO2
Г CaSiO3, SiH4
9.76 Визначте та вкажіть формулу речовини X у схемі перетворень: 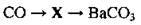
А К2СO3
Б КНСО3
В Н2СO3
Г CO2
9.77 Позначте формули речовин, які взаємодіють з натрій карбонатом: 1) ВаО; 2) ВаСO3; 3) Ва(ОН)2; 4) НСl; 5) КСl; 6) HNO3
А 1, 3, 4
Б 3, 4, 6
В 1, 3, 6
Г 2, 4, 6
9.78 Установіть відповідність між реагентами і продуктами реакцій
Реагенти: | Продукти реакції: |
| А кальцій гідрогенкарбонат Б кальцій гідрогенкарбонат і вода В кальцій карбонат і вода Г кальцій карбонат Д кальцій карбонат, карбон(ІV) оксид і вода |
9.79 Укажіть формулу кристалічної соди
A Na2CO3 · Н2O
Б К2СO3 · 2Н2О
В Na2CO3 · 5Н2O
Г Na2CO3 · 10Н2O
9.80 Укажіть рівняння реакції, яке відповідає скороченій йонній формі 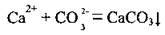
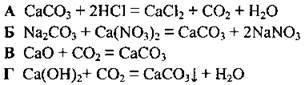
9.81 Позначте речовини, які використовують для виробництва звичайного скла
А кварц або пісок, кальцій карбонат і натрій карбонат
Б магній карбонат, пісок, калій гідрогенкарбонат
В силіцій(ІV) оксид, кальцій карбонат, натрій гідрогенкарбонат
Г кальцій карбонат, магній карбонат, силіцій(ІV) оксид
9.82 Позначте формули речовин, які взаємодіють з амоній карбонатом: 1) H2SO4; 2) КОН; 3) СuО; 4) NaCl; 5) ВаСl2; 6) СаСO3
А 1, 2, 4
Б 2, 4, 6
В 3, 4, 5
Г 1, 2, 5
9.83 Установіть послідовність використання реагентів, необхідних для здійснення таких перетворень:
Чадний газ → карбон(ІV) оксид → кальцій карбонат → карбон(ІV) оксид → кальцій гідрогенкарбонат
А кальцій гідроксид
Б кальцій оксид
В кисень
Г хлоридна кислота
9.84 Укажіть формулу реактиву, за допомогою якого можна розпізнати розчини калій хлориду, калій броміду, калій йодиду і калій флуориду
A Ba(NO3)2
Б Cu(NO3)2
В KNO3
Г AgNO3
9.85 Укажіть формулу кислоти, яка реагує із силіцій(ІV) оксидом
A HF
Б НСl
В НВr
Г HNO3(конц.)
9.86 Укажіть речовину, взаємодію якої з хлором відносять до реакцій заміщення
А Аl
Б Р
В KF
Г КВr
9.87 Укажіть молярну масу продукту реакції фосфору з надлишком галогену, йон якого містить на 18 електронів менше, ніж елемент 5-го періоду із завершеним електронним шаром
А 271 г/моль
Б 431 г/моль
В 137,5 г/моль
Г 208,5 г/моль